Hòa tan hết 11,2 gam Fe vào lượng vừa đủ dung dịch axit sunfuric loãng, sau phản ứng, thu được V lít khí duy nhất (đktc). Giá trị của V là
A. 10,0
B. 14,0
C. 4,48
D. 19,8
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phản ứng: Fe + H2SO4 → FeSO4 + H2↑.
Để cho nFe = 0,2 mol ⇒ nH2 = 0,2 mol ⇒ V = 0,2 × 22,4 = 4,48 lít.
Đáp án C

Đáp án C
Lời giải : số mol của Fe :0,2 mol
Ta có Fe + 2HCl → FeCl2 + H2
Thì số mol của H2 : 0,2 mol nên V=4,48 lít

$n_{Al} = \dfrac{8,1}{27} = 0,3(mol)$
$2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
$FeO + H_2SO_4 \to FeSO_4 + H_2O$
$n_{H_2} = \dfrac{3}{2}n_{Al} = 0,45(mol)$
$V = 0,45.22,4 = 10,08(lít)$
\(n_{Al}=\frac{8,1}{27}=0,3mol\\ 2Al+3H_2SO_4\rightarrow Al_2(SO_4)_3 +3H_2 n_{H_2}=0,45mol\\ V=10,08l\)

Đáp án B
Đặt nH2 = x => nH2SO4 = x
BTKL: mKL + mH2SO4 = m muối + mH2
8,975 + 98x = 32,975 + 2x => x = 0,25 mol
=> V = 5,6 lít

Đáp án B
Đặt nH2 = x => nH2SO4 = x
BTKL: mKL + mH2SO4 = m muối + mH2
8,975 + 98x = 32,975 + 2x => x = 0,25 mol
=> V = 5,6 lít

Đáp án B
Đặt nH2 = x => nH2SO4 = x
BTKL: mKL + mH2SO4 = m muối + mH2
8,975 + 98x = 32,975 + 2x => x = 0,25 mol
=> V = 5,6 lít

Đáp án B
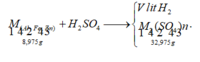
B T K L : n S O 4 2 - = m m u o i - m k l 96 = 32 , 975 - 8 , 975 96 = 0 , 25 ( m o l ) n H 2 = n S O 4 2 - = 0 , 25 m o l ⇒ V H 2 = 0 , 25 . 22 , 4 = 5 , 6 ( l í t )

PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\) (1)
\(2Fe+6H_2SO_{4\left(đ\right)}\underrightarrow{t^o}Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\) (2)
\(5SO_2+2KMnO_4+2H_2O\rightarrow2MnSO_4+K_2SO_4+2H_2SO_4\) (3)
Ta có: \(n_{H_2}=0,2\left(mol\right)\)
Theo PT (1): \(n_{Fe}=n_{H_2}=0,2\left(mol\right)\)
Theo PT (2): \(n_{SO_2}=\dfrac{3}{2}n_{Fe}=0,3\left(mol\right)\)
\(\Rightarrow V_{SO_2}=0,3.22,4=6,72\left(l\right)\)
Theo PT (3): \(n_{KMnO_4}=\dfrac{2}{5}n_{SO_2}=0,12\left(mol\right)\)
\(\Rightarrow V_{KMnO_4}=\dfrac{0,12}{2}=0,06\left(l\right)\)
Bạn tham khảo nhé!
Chọn đáp án C
Phản ứng: Fe + H2SO4 → FeSO4 + H2↑.
Để cho nFe = 0,2 mol ⇒ nH2 = 0,2 mol ⇒ V = 0,2 × 22,4 = 4,48 lít.
Chọn đáp án C