Trước đây người ta thường trộn vào xăng chất Pb(C2H5)4. Khi đốt cháy xăng bằng dung dịch H2SO4 loãng thu được dung dịch Y chỉ chứa 2 muối sunfat có khối lượng 130,4 gam và 0,5 mol khí H2. Cho Y tác dụng với dung dịch Ba(OH)2 dư (trong điều kiện không có không khí) thu được m gam kết tủa.Biết hidroxit của A không tan trong kiềm mạnh và nếu lấy 63 gam X thì có thể điều chế được tối đa 55 gam hỗn hợp kim loại.Giá trị của m gần nhất với:
A. 280
B. 290
C. 300
D. 310

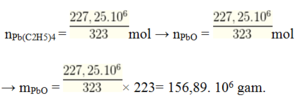


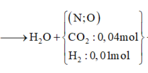
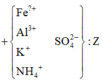
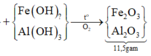
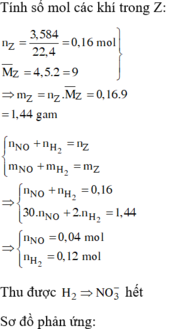

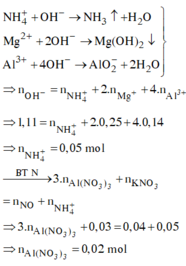


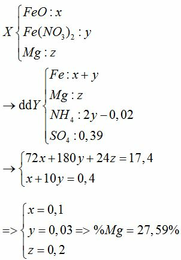

Đáp án A
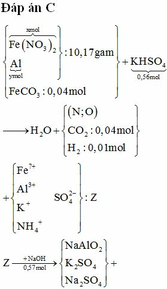
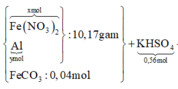
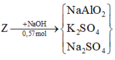
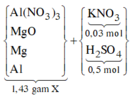
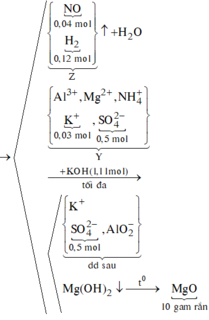
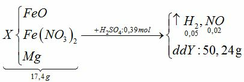
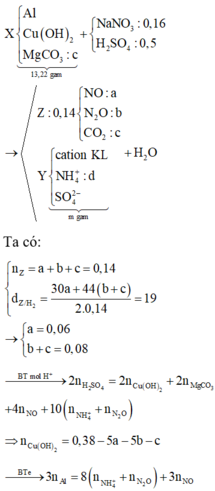
X(Fe, A, oxit sắt) → Dung dịch Y chỉ chứa 2 muối sunfat: 130,4 gam + 0,5 mol H2 + H2O
Coi hỗn hợp ban đầu gồm Fe, A, O. Trong 63 gam X thì mO =8 gam
→ mkim loại = 6,875mO
Trong hỗn hợp X gọi số mol Fe, A, O lần lượt là x, y,z
Ta có nH2O= nO = z mol, nH2SO4 = z + 0,5
Vì dung dịch chỉ chứa 2 muối sunfat → dung dịch Y chứa An+: x mol, Fe2+: y mol và SO42-: 0,5 + z mol
→ mkim loại = 6,875.16z = 110z gam
→ mSO42- = 130,4 - 110z= 96.(z + 0,5)
→ z=0,4 mol
Kết tủa thu được gồm Fe(OH)2: y mol, A(OH)n: x mol, BaSO4: 0,5 + z mol
Bảo toàn điện tích trong dung dịch Y → 2y + xn = 2.(0, 5+z) → nOH- = 1 + 2z
mkết tủa = mkim loại + mOH- + mBaSO4 = 110z + 17.(1+2z) + 233.(0,5+z) = 377z + 133,5 = 284,5 gam.