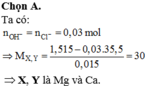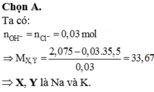Cho 3,82 gam hỗn hợp G gồm 2 muối cacbonat của 2 kim loại kiềm (thuộc hai chu kì liên tiếp trong bảng tuần hoàn) vào dung dịch H 2 S O 4 2M dư thu được 1,32 gam khí không màu bay ra. Tính % khối lượng của từng muối trong G.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.




Gọi công thức trung bình của hai muối là: M ¯ 2 CO 3
Cho từ từ hỗn hợp muối cacbonat nên ta có phản ứng:
CO 3 2 - + 2 H + → CO 2 + H 2 O
Sau khi phản ứng với dung dịch axit, thêm Ba(OH)2 dư vào Y thấy xuất hiện kết tủa H+ hết và dư CO 3 2 -
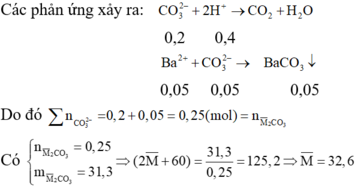
Vậy hai kim loại cần tìm là Na và K
Đáp án B.

Đáp án B
Gọi công thức trung bình của hai muối là: M2CO3.
Sau khi phản ứng với dung dịch axit, thêm Ba(OH)2 dư vào Y thấy xuất hiện kết tủa à H+ hết và dư CO32-
Các phản ứng xảy ra: CO32- + 2H+ → CO2 + H2O
0,2 0,4
CO32-dư + Ba2+ → BaCO3
0,05 0,05 0,05

Đặt tên chung của 2 kim loại A,B đó là Z \(\left(M_A< M_Z< M_B\right)\)
\(2M+2HCl\rightarrow2MCl+H_2\\ n_{HCl}=n_M=n_{Cl^-}=\dfrac{18,65-8}{35,5}=0,3\left(mol\right)\\ \Rightarrow M_Z=\dfrac{8}{0,3}\approx26,667\left(\dfrac{g}{mol}\right)\\ \Rightarrow\left\{{}\begin{matrix}A:Natri\left(Na=23\right)\\B:Kali\left(K=39\right)\end{matrix}\right.\)

Gọi công thức muối cacbonat trung hòa của 2 kim loại kiềm cần tìm là R2CO3
\(R_2CO_3+2HCl\rightarrow2RCl+H_2O+CO_2\)
\(n_{CO_2}=n_{R_2CO_3}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ \Rightarrow M_{R_2CO_3}=2M_R+60=\dfrac{9,1}{0,1}=91\\ \Rightarrow M_R=15,5\)
Do 2 kim loại kiềm ở chu kì liên tiếp nhau
=> 2 kim loại đó là Li, Na