Cho 22 gam hỗn hợp X gồm Al và Fe phản ứng hoàn toàn với 500 ml dung dịch HCl1,2 M. Chứng minh hỗn hợp X không tan hết.
A. Có
B. Không
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) \(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
\(n_S=\dfrac{1,6}{32}=0,05\left(mol\right)\)
PTHH: Fe + S --to--> FeS
0,05<-0,05-->0,05
Fe + 2HCl --> FeCl2 + H2
0,05->0,1---->0,05-->0,05
FeS + 2HCl --> FeCl2 + H2S
0,05-->0,1----->0,05--->0,05
=> \(\%V_{H_2S}=\%V_{H_2}=\dfrac{0,05}{0,05+0,05}.100\%=50\%\)
b)
nNaOH = 0,3 (mol)
- Gọi số mol HCl trong B là a (mol)
PTHH: NaOH + HCl --> NaCl + H2O
a<-----a
FeCl2 + 2NaOH --> Fe(OH)2 + 2NaCl
0,1---->0,2
=> a + 0,2 = 0,3
=> a = 0,1 (mol)
\(C_{M\left(FeCl_2\left(B\right)\right)}=\dfrac{0,1}{0,5}=0,2M\)
\(C_{M\left(HCl\left(B\right)\right)}=\dfrac{0,1}{0,5}=0,2M\)
nHCl(bđ) = 0,3 (mol)
=> \(C_{M\left(dd.HCl\left(bđ\right)\right)}=\dfrac{0,3}{0,5}=0,6M\)

Bắt đầu xuất hiện kết tủa nghĩa là: NaOH đầu tiên sẽ trung hòa HCl dư trước
NaOH + HCldư → NaCl + H2O
0,2 ←0,2
→ 2V1 = 0,2 → V1 = 0,1
Đến khi kết tủa không thay đổi khối lượng thì khi đó kết tủa bị hòa tan hết.
3NaOH + AlCl3 → 3NaCl + Al(OH)3↓
3x ←x → x
NaOH + Al(OH)3 → NaAlO2 + 2H2O
x ←x
→ 0,2 + 4x = 0,6.2 → x = 0,25
=> y = 0,025
=> m = 17,75g

Chú ý: Cr không tan trong kiềm loãng.
Hướng dẫn giải:
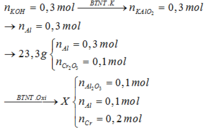
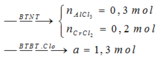
Đáp án A
Với bài này, để chứng minh hỗn hợp X không tan hết ta có thể làm như sau:
Cách 1: Ta có các phản ứng xảy ra như sau:
Nhân 2 vế của bất phương trình với 2: 0,78 < 2(a + b) < 1,62
Ta có: 2(a + b) > 0,78
Theo (1) và (2): nHCl = 3a + 2b = 0,5.1,2 = 0,6 mol.
Mà 3a + 2b > 2(a + b) > 0,78 nên naxit cần để hòa tan hết kim loại > 0,78
n a x i t thực tế = 0,6 nên sau phản ứng, kim loại chưa tan hết.
Cách 2: Các phản ứng xảy ra:
Gọi a, b là số mol của Al và Fe. Ta có 27a + 56b = 22
nHCl cần để hòa tan hết kim loại = 3a+2b
Mà nHCl thực tế = 0,6 < 0,78 nên sau phản ứng kim loại chưa bị hòa tan hết.
Đáp án B