Dung dịch X chứa 0,15 mol Fe 3 + ; x mol Al 3 + ; 0,25 mol SO 4 2 - và y mol Cl - . Cho 710 ml dung dịch Ba(OH)2 1M vào dung dịch X thu được 92,24 gam kết tủa. Giá trị của x và y lần lượt là :
A. 0,23 và 0,64
B. 0,5 và 0,45
C. 0,3 và 0,85
D. 0,3 và 0,45

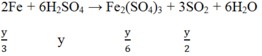
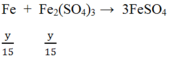
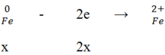


Đáp án C
Như vậy dung dịch sau phản ứng có chứa các ion Ba 2 + , Cl - , Al OH 4 - . Áp dụng bảo toàn điện tích cho dung dịch sau phản ứng, ta có :
→ y = 0,85
Áp dụng bảo toàn điện tích cho dung dịch ban đầu, ta có
→ x = 0,3