Nguyên tố X hoá hợp với H cho hợp chất XH 4 Oxit cao nhất của nó chứa 53,3% oxi về khối lượng.
Tính số khối của X (coi số khối trùng với nguyên tử khối).
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Nguyên tố X hợp với hidro cho hợp chất XH4 => Oxit cao nhất của X là XO2
Ta có : \(\frac{16\cdot2}{X+16\cdot2}\cdot100\%=53,3\%\)
\(\Rightarrow X=28\)(Silic)

Hợp chất khí với hidro của một nguyên tố là RH4, theo bảng tuần hoàn suy ra công thức oxit cao nhất của R là RO2, trong phân tử RO2 có 53,3% oxit về khối lượng nên R có 100% - 53,3% = 46,7% về khối lượng.
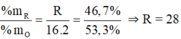
Vậy R là Si. Công thức phân tử là SiH4 và SiO2.

RH4 -> RO2
%R= 53,3% => %O = 100-53,3= 46,7%
\(\dfrac{R}{53,3}\)=\(\dfrac{32}{46,7}\)
giải tìm R

Hợp chất khí với hidro của nguyên tố R là RH2. Oxit cao nhất của nguyên tố R chứa 60% oxi về khối lượng. Xác định nguyên tố R
===============
Hợp chất khí với hidro của nguyên tố R là RH2.
=> công thức với Oxi là RO
=>R/(R+16).100%=60%
<=>R/(R+16)=0,6
<=>0,4R=9,6
<=>R=24
=>R la Mg

a)
Do R có hóa trị III trong hợp chất với hidro
=> R có hóa trị V trong oxit cao nhất
Oxit cao nhất của R là: R2O5
b) Có \(\%O=\dfrac{16.5}{2.M_R+16.5}.100\%=74,074\%\)
=> MR = 14
=> R là N(Nitơ)

Công thức oxit cao nhất là RO2
Có \(\dfrac{32}{M_R+32}.100\%=53,3\%=>M_R=28\left(Si\right)\)

Đáp án B
Công thức hợp chất khí với hiđro là RH4 => Hóa trị của R trong hợp chất khí với hiđro là 4 => Hóa trị
của R trong oxit cao nhất = 8 - 4 = 4 =>Công thức oxit cao nhất là RO2
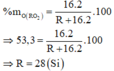
R là Si(silic)
Vì nguyên tố X hợp với hiđro cho hợp chất XH 4 nên nguyên tố đó thuộc nhóm IVA. Oxit cao nhất của nó sẽ là XO 2
Theo đề bài ta có : m O / m XO 2 = 53,3/100
Nguyên tử khối của oxi là 16. Gọi X là nguyên tử khối của X, ta sẽ có :
Từ đó ta có : 53,3.(x+32) = 100.32
x + 32 = 100 x 32/53,3 = 60
Nguyên tử khối của X : x = 60 - 32 = 28.
X thuộc nhóm IVA, có số khối là 28. Vậy nguyên tố đó là silic (Si)