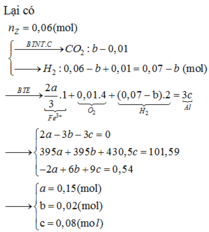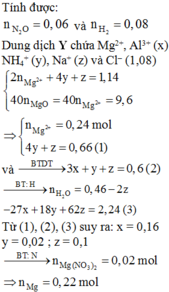Rắc bột nhôm đun nóng vào lọ chứa khí C l 2 thu được 0,1 mol muối và Al còn dư. Hỗn hợp sau phản ứng cho tác dụng với dung dịch HCl (dư) thấy có tạo ra 3,36 lít khí H 2 (đktc). Xác định tỉ lệ % lượng Al tác dụng với clo so với lượng Al ban đầu
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

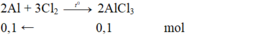


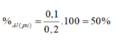

- Hỗn hợp rắn sau pư gồm: Fe và FeCl3.
Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
BT e, có: \(2n_{Fe}=2n_{H_2}\Rightarrow n_{Fe}=0,1\left(mol\right)\)
BTNT Fe, có: \(n_{FeCl_3}=n_{Fe\left(OH\right)_3}=0,03\left(mol\right)\) = nFe (pư)
BTNT Fe, có: nFe (ban đầu) = nFe + nFeCl3 = 0,13 (mol)
\(\Rightarrow H\%=\dfrac{0,03}{0,13}.100\%\approx23,077\%\)

1. Gọi chung hh 2 KL trên là A.
BT e, có: nA = 2nH2 ⇒ nH2 = 0,05 (mol)
⇒ VH2 = 0,05.22,4 = 1,12 (l)
2. Ta có: \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
BT e, có: 3nAl = 2nH2 ⇒ nAl = 0,1 (mol)
\(\Rightarrow m_{Al_2O_3}=7,8-m_{Al}=5,1\left(g\right)\)
\(\Rightarrow\%m_{Al_2O_3}=\dfrac{5,1}{7,8}.100\%\approx65,38\%\)

Khối lượng từng phần là : ![]()
Phản ứng nhiệt nhôm: 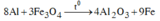
=> Hỗn hợp X gồm Al2O3, Fe, Al dư, Fe3O4 dư
Xét phần hai:
X tác dụng với dung dịch HNO3 cũng chính là hỗn hợp ban đầu Al (a mol) và Fe3O4 (b mol) tác dụng với dung dịch HNO3
![]()
Quy đổi hỗn hợp ban đầu thành Al: a mol; Fe: 3b mol; O:4b mol
Sơ đồ phản ứng:
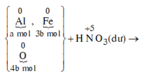
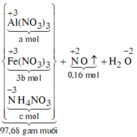
![]()
![]()
![]()
![]()
![]() ]
]
![]()
![]() c = 0,0375 mol
c = 0,0375 mol
-Xét phần một:
Số mol H2 thu được là: ![]()
Sơ đồ phản ứng tạo khí H2 : 
![]()
![]()
![]()
![]()
-Xét phản ứng nhiệt nhôm:
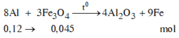
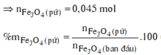
![]()
Đáp án B.

Đáp án A
Cho toàn bộ Y tác dụng với 0,9 mol HCl thu được 0,15 mol H2 và 0,06 mol Cu không tan
Vậy dung dịch X chứa AlCl3 0,16 mol, CuCl2 0,04 mol, CrCl3 0,06 mol
![]()
Bảo toàn Cl:
![]() = 0,16
= 0,16
![]() = 1,12 mol
= 1,12 mol