Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Ta có sơ đồ phản ứng:
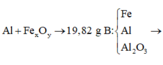
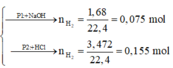
Phần 1:
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑
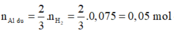
![]()
Phần 2:
2Al + 6HCl → 2AlCl3 + 3H2↑ (1)
0,05 → 0,075
Fe + 2HCl → FeCl2 + H2↑ (2)
![]()
![]()
![]()
![]()
Ta có phương trình phản ứng:
![]()
Khối lượng các chất trong 1 phần hỗn hợp B là 19,82/2 = 9,91 g
![]()
![]()
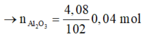
Ta có:
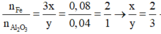
=> Oxit sắt cần tìm là Fe2O3

Đáp án C
Xét phần 1: quy Y về Fe, Cr, Al và O ![]()
-Xét phần 2: bảo toàn nguyên tố Hidro: ![]()
=> bảo toàn nguyên tố Oxi:
![]()
Quay lại phần 1, bảo toàn electron: ![]()
Xét phần 2: bảo toàn khối lượng: ![]()
Lại có: ![]() đều phản ứng với NaOH theo dạng:
đều phản ứng với NaOH theo dạng:
![]()
![]()
= (0,04 + 2a) mol
Bảo toàn nguyên tố Al và Cr: ![]()
Bảo toàn nguyên tố Natri: ![]()
Bảo toàn khối lượng:![]()
![]()
![]()
![]()
![]()

Đáp án C


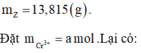
![]()
đều phản ứng với NaOH theo dạng:
![]()
![]()
Bảo toàn nguyên tố Al và Cr
![]()
Bảo toàn nguyên tố Natri: ![]()
Bảo toàn khối lượng:
13,815 + 40x (0,27 + a) = 6,6 + 0,25 × 58,5 + 0,02 × 82+ 107a + 18 × (0.04 + 2a)
=> a = 0,01 mol => x = 0,27 + 0,01 = 0,28 mol

Đáp án B.
![]()
Giả sử Z + H2SO4 → dung dịch muối tạo thành chỉ có Fe2(SO4)3:
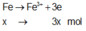
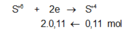
![]()
![]()
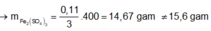
→ muối thu được gồm FeSO4 và Fe2(SO4)3.
Ta có sơ đồ phản ứng:
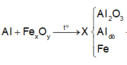
→ + N a O H d ư
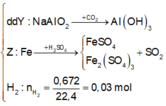

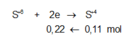
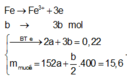
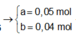
![]()
X tác dụng được với dung dịch NaOH tạo khí H2 →Al dư.
![]()
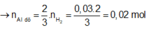
![]()
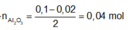
![]()
![]()
![]()
![]()

Đáp án A
phần 1: 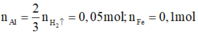
phản ứng : 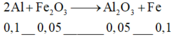
![]()
![]()
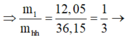
lượng phần 2 gấp đối phần 1
phần 2: 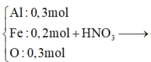
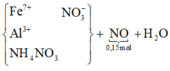
Ta có: ![]()
![]()
![]()
=>bảo toàn nguyên tố H có: ![]()
bảo toàn khối lượng:![]()
![]()



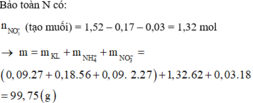
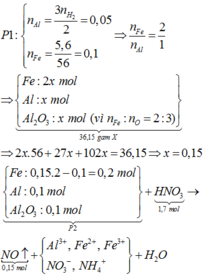
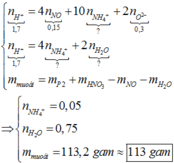
1. Gọi chung hh 2 KL trên là A.
BT e, có: nA = 2nH2 ⇒ nH2 = 0,05 (mol)
⇒ VH2 = 0,05.22,4 = 1,12 (l)
2. Ta có: \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
BT e, có: 3nAl = 2nH2 ⇒ nAl = 0,1 (mol)
\(\Rightarrow m_{Al_2O_3}=7,8-m_{Al}=5,1\left(g\right)\)
\(\Rightarrow\%m_{Al_2O_3}=\dfrac{5,1}{7,8}.100\%\approx65,38\%\)