Đốt hoàn toàn 24 ml hỗn hợp axetilen và metan phải dùng 54 ml oxi (các thể tích khí đo ở đktc). Thể tích khí C O 2 sinh ra là
A. 24 ml.
B. 30 ml.
C. 36 ml.
D. 42 ml.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(2C_2H_2\left(x\right)+5O_2\left(2,5x\right)\rightarrow4CO_2\left(2x\right)+2H_2O\)
\(CH_4\left(y\right)+2O_2\left(2y\right)\rightarrow CO_2\left(y\right)+2H_2O\)
Ta có : \(x+y=24\Rightarrow y=24-x\)
\(2,5x+2y=54\)
\(\Rightarrow2,5x+2\left(24-x\right)=54\)
\(\Rightarrow x=12ml\)
\(\Rightarrow y=12ml\)
a) \(\%C_2H_2=12.100\%:24=50\%\)
\(\%CH_4=100\%-50\%=50\%\)
b)\(V_{CO_2}=2x+y=36\left(ml\right)\)

\(28ml=0,028l\)
\(67,2ml=0,0672l\)
Giả sử ta đo ở đktc
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=x\\n_{C_2H_2}=y\end{matrix}\right.\)
\(n_{hh}=\dfrac{0,028}{22,4}=0,00125mol\)
\(n_{O_2}=\dfrac{0,0672}{22,4}=0,003mol\)
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
x 2x ( mol )
\(2C_2H_2+5O_2\rightarrow\left(t^o\right)4CO_2+2H_2O\)
y 5/2 y ( mol )
Ta có:
\(\left\{{}\begin{matrix}x+y=0,00125\\2x+\dfrac{5}{2}y=0,003\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,00025\\y=0,001\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,00025}{0,00125}.100=20\%\\\%V_{C_2H_2}=100\%-20\%=80\%\end{matrix}\right.\)
=> Chọn A

Bài 4. Đốt cháy 28 ml hỗn hợp khí metan và axetilen cần phải dùng 67,2 ml khí oxi.
a) Tính phần trăm thể tích của mỗi khí trong hỗn hợp.
b) Tính thể tích khí CO2 sinh ra.
(Các thể tích khí đo ở cùng điểu kiện nhiệt độ và áp suất).
Lời giải:
Đối với chất khí, trong cùng điều kiện về nhiệt độ và áp suất, tỉ lệ số mol trong phương trình phản ứng cũng là tỉ lệ về thể tích các khí.
a) Gọi thế tích của CH4 và C2H2 lần lượt là x, у (ml).
Phương trình phản ứng: CH4 + 2O2 → CO2 + 2H2O
p.ư: x -> 2x x (ml)
2C2H2 + 5O2 → 4CO2 + 2H2O
p.ư: у -> 2,5y 2y (ml)
Theo thể tích hỗn hợp và thể tích oxi, ta có hệ phương trình:
Giải (1) và (2), ta được x = 5,6ml và y = 22,4ml.
% =
x 100% = 20%; %
= 100% - 20% = 80%
b) Thể tích khí khí C02 sinh ra = x + 2y = 5,6 + 2 x 22,4 = 50,4ml.

\(V_{CH_4} = a(ml) ; V_{C_2H_2} = b(ml)\\ \Rightarrow a + b = 28(1)\\ CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ 2C_2H_2 + 5O_2 \xrightarrow{t^o} 4CO_2 + 2H_2O\\ V_{O_2} = 2a + \dfrac{5}{2}b = 67,2(2)\\ (1)(2) \Rightarrow a = 5,6 ; b = 22,4\\ V_{CH_4} = 5,6(ml) ; V_{C_2H_2} = 22,4(ml)\)

1. Khi đun nóng A có mặt chất xúc tác Ni, chỉ còn lại 1 chất khí duy nhất. Vậy ankan và anken trong A có cùng số nguyên tử cacbon.
Giả sử trong 100 ml A có x mol C n H 2 n + 2 ; y mol C n H 2 n và z mol H 2 .
x + y + z = 100 (1)
Khi đốt cháy hoàn toàn 100 ml A :
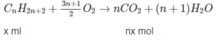
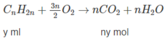
2 H 2 + O 2 → 2 H 2 O
Thể tích C O 2 : n(x + y) = 210 (2)
Khi đun nóng A có mặt chất xúc tác Ni:
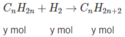
x + y = 70 (3)
y = z (4)
Giải hộ phương trình, tìm được n = 3; x = 40 ; y = z = 30.
Thành phần thể tích của hỗn hợp A là : C 3 H 8 : 40% ; C 3 H 6 : 30%; H 2 : 30%
2. Thể tích O 2 là 350 ml.

Đáp án B
Đặt CTTQ của amin là CnH2n+3N.
Đặt a, b, c lần lượt là thể tích của C2H2, C3H4 và amin A.
a + b + c = 100 ml (1)
= a + 2b + nc + 1,5c = 305 ml (2)
= 2a + 3b + nc + 0,5c =630 – 305 = 325 ml (3)
Lấy (3) trừ (2) được a + b – c = 325 – 305 = 20 ml (4)
Từ (1) và (4) suy ra
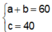
Thay vào (2) ta được 60 + b + 40n + 1,5.40 = 305
→ b + 40n = 185
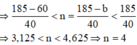
CTPT của A là C4H11N mà A phản ứng với HNO2 tạo khí N2 nên A có nhóm amin gần với C bậc 1.
Các đồng phân của A là:
CH3CH2CH2CH2NH2
(CH3)2CHCH2NH2
CH3CH2NH(CH3)NH2
Vậy có 3 công thức thỏa mãn.

a, \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
Ta có: \(n_{CH_4}+n_{C_2H_2}=\dfrac{0,028}{22,4}=0,00125\left(mol\right)\left(1\right)\)
Theo PT: \(n_{O_2}=2n_{CH_4}+\dfrac{5}{2}n_{C_2H_2}=\dfrac{0,0672}{22,4}=0,003\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CH_4}=0,00025\left(mol\right)\\n_{C_2H_2}=0,001\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,00025.22,4}{0,028}.100\%=20\%\\\%V_{C_2H_2}=80\%\end{matrix}\right.\)
b, Theo PT: \(n_{CO_2}=n_{CH_4}+2n_{C_2H_2}=0,00225\left(mol\right)\)
\(\Rightarrow V_{CO_2}=0,00225.22,4=0,0504\left(l\right)\)

Đáp án B
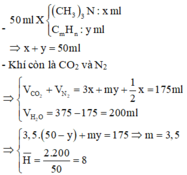
=> 2 hidrocacbon có số nguyên tử C là 3 và 4 và có 1 hidrocacbon có số nguyên tử H nhỏ hơn 8
- Kết hợp đáp án suy ra 2 hidrocacbon là C 3 H 6 và C 4 H 8
Đáp án: C