Hòa tan hoàn toàn 6,5g kẽm trong x gam dung dịch axit clohiđric (HCl) sau phản ứng thu đc 13,6g kẽm clorua (ZnCl2) và 0,2g khí hidro
a) viết phương trình chữ của phản ứng
b) tính khối lượng HCl cần dùng
c) tính x biết lượng axit đã dùng dư 10%
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a,PTHH:Zn+2HCl\to ZnCl_2+H_2\\ b,\text {Bảo toàn KL: }m_{Zn}+m_{HCl}=m_{ZnCl_2}+m_{H_2}\\ \Rightarrow m_{ZnCl_2}=6,5+7,3-0,2=13,6(g)\)

Nzn=0,1mol
a) có pt : Zn + 2Hcl -> ZnCl2 + H2
1 -> 2 -> 1 -> 1 mol
0,1-> 0,2 -> 0,1 -> o,1 mol
b) số Hcl đã dùng khi pứ là :
0,2 . 36,5= 7,3
-> số gam hcl dư là 10,95- 7,3=3,65(g)
c)mZnCl2=0,1 . 136=13,6g

a. \(n_{Zn}=\dfrac{6.5}{65}=0,1\left(mol\right)\)
PTHH : Zn + 2HCl -> ZnCl2 + H2
0,1 0,2 0,1
b. \(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
c. \(m_{HCl}=0,2.36,5=7,3\left(g\right)\)
\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,1
\(V_{H_2}=0,1\cdot22,4=2,24l\)
\(m_{HCl}=0,2\cdot36,5=7,3g\)

\(a.Zn+2HCl\rightarrow ZnCl_2+H_2\\ b.n_{Zn}=\dfrac{65}{65}=1\left(mol\right)\\ n_{ZnCl_2}=n_{Zn}=1\left(mol\right)\\ \Rightarrow m_{ZnCl_2}=1.136=136\left(g\right)\\ c.n_{H_2}=n_{Zn}=1\left(mol\right)\\ \Rightarrow V_{H_2}=1.22,4=22,4\left(l\right)\)

a.b.c.\(n_{Zn}=\dfrac{m}{M}=\dfrac{13}{65}=0,2mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,2 0,2 0,2 ( mol )
\(m_{ZnCl_2}=n.M=0,2.136=27,2g\)
\(V_{H_2}=n.22,4=0,2.22,4=4,48l\)
d.\(n_{CuO}=\dfrac{m}{M}=\dfrac{32}{80}=0,4mol\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,4 > 0,2 ( mol )
0,2 0,2 0,2 ( mol )
\(m_{chất.rắn}=m_{CuO\left(dư\right)}+m_{Cu}=0,2.80+0,2.64=16+12,8=28,8g\)
\(\%m_{CuO}=\dfrac{16}{28,8}.100=55,55\%\)
\(\%m_{Cu}=100\%-55,55\%=44,45\%\)

\(a.Zn+2HCl\rightarrow ZnCl_2+H_2\\ n_{Zn}=n_{ZnCl_2}=n_{H_2}=0,25\left(mol\right)\\ \Rightarrow m_{Zn}=0,25.65=16,25\left(g\right)\\ m_{ZnCl_2}=0,25.136=34\left(g\right)\\ b.FeO+H_2-^{t^o}\rightarrow Fe+H_2O\\ Tacó:n_{Fe}=n_{H_2}=0,25\left(mol\right)\\ \Rightarrow m_{Fe}=0,25.56=14\left(g\right)\)

\(n_{Zn}=\dfrac{13}{65}=0,2(mol)\\ a,PTHH:Zn+2HCl\to ZnCl_2+H_2\\ b,n_{HCl}=2n_{Zn}=0,4(mol)\\ \Rightarrow m_{HCl}=0,4.36,5=14,6(g)\\ c,n_{H_2}=n_{Zn}=0,2(mol)\\ \Rightarrow V_{H_2}=0,2.22,4=4,48(l)\)
b) mHCl = 14,6 (g)
V H2 = 4,48 (l)
Giải thích các bước:
a) PTHH: Zn + 2HCl → ZnCl2 + H2↑
b) nZn = 13 : 65 = 0,2 mol
Theo PTHH: nHCl = 2.nZn = 0,4 mol
mHCl = 0,4 . 36,5 = 14,6(g)
c) nH2 = nZn = 0,2 mol
VH2 = 0,2 . 22,4 = 4,48 (l)

`a)PTHH:`
`Zn + 2HCl -> ZnCl_2 + H_2`
`0,1` `0,2` `0,1` `0,1` `(mol)`
`n_[HCl]=0,2.1=0,2(mol)`
`=>m_[Zn]=0,1.65=6,5(g)`
`b)m_[dd HCl]=1,1.200=220(g)`
`=>C%_[ZnCl_2]=[0,1.136]/[6,5+220-0,1.2].100~~6%`
\(a,n_{HCl}=0,2.1=0,2\left(mol\right)\)
PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
0,1<--0,2------>0,1------->0,1
\(\rightarrow m_{Zn}=0,1.65=6,5\left(g\right)\)
\(b,m_{ddHCl}=200.1,1=220\left(g\right)\)
\(\rightarrow m_{dd}=220+6,5-0,1.2=226,3\left(g\right)\\ \rightarrow C\%_{ZnCl_2}=\dfrac{0,1.136}{226,3}.100\%=6\%\)

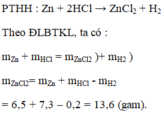
a, Kẽm + Axit clohiđric → Kẽm clorua + hiđro
b, Theo ĐLBT KL, có:
mZn + mHCl = mZnCl2 + mH2
⇒ mHCl = 13,6 + 0,2 - 6,5 = 7,3 (g)
c, Do lượng axit dùng dư 10%
⇒ x - 0,1x = 7,3 ⇒ x = 73/9 (g)
Bạn tham khảo nhé!