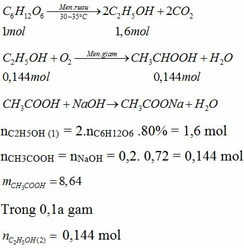
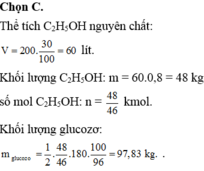
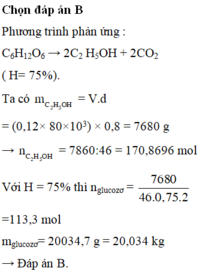Tính khối lượng rượu etylic cần dùng để điều chế 200 gam dung dịch CH3COOH trên bằng phương pháp lên men với hiệu suất 80%.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


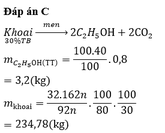
Đáp án B.
m k h o a i = 100 . 0 , 4 . 0 , 8 . 162 46 . 2 . 0 , 8 . 0 , 3 = 234 , 782 k g

a) n Zn = 6,5/65 = 0,1(mol)
Zn + 2CH3COOH $\to$ (CH3COO)2Zn + H2
Theo PTHH :
n CH3COOH = 2n Zn =0,2(mol)
C% CH3COOH = 0,2.60/200 .100% = 6%
b) n H2 = n Zn = 0,1(mol)
=> m dd sau pư = 6,5 + 200 - 0,1.2 = 206,3 gam
Theo PTHH : n (CH3COO)2Zn = n Zn = 0,1(mol)
=> C% (CH3COO)2Zn = 0,1.183/206,3 .100% = 8,87%
c)
C2H5OH + O2 $\xrightarrow{men\ giấm}$ CH3COOH + H2O
n C2H5OH pư = n CH3COOH = 0,2(mol)
=> m C2H5OH cần dùng = 0,2.46/80% = 11,5 gam
a) nZn=0,1(mol)
PTHH: Zn + 2 CH3COOH -> (CH3COO)2Zn + H2
0,1_______0,2_________0,1_____________0,1(mol)
mCH3COOH=0,2.60=12(g)
=> C%ddCH3COOH=(12/200).100=6%
b) mdd(CH3COO)2Zn= 6,5+200-0,1.2=206,3(g)
m(CH3COO)2Zn= 183 x 0,1=18,3(g)
=>C%dd(CH3COO)2Zn= (18,3/206,3).100=8,871%
c) C2H5OH + O2 -men giấm-> CH3COOH + H2O
nC2H5OH(LT)=nCH3COOH=0,2(mol)
=> nC2H5OH(TT)=0,2 : 80%= 0,25(mol)
=>mC2H5OH=0,25 x 46= 11,5(g)