Cho 2,8 gam bột sắt phản ứng hoàn toàn với khí Clo dư sau phản ứng khối lượng muối thu được là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Phương trình hoá học : 2Fe + 3 Cl 2 → t ° FeCl 3
Theo định luật bảo toàn khối lượng :
m Fe + m Cl 2 = m FeCl 3
m Cl 2 = m FeCl 3 - m Fe = 16,25 - 5,6 = 10,65g

Đ á p á n D A l F e x O y → t o , H = 100 % Y → N a O H H 2 ⏟ o , 15 m o l ⇒ Y : A l , F e A l 2 O 3 Z c h ứ a F e V ớ i Y : B T e : 3 n A l = 2 n H 2 V ớ i Z : 3 n F e = 2 n S O 2 n S O 4 2 - t ạ o m u ố i = n S O 2 = x 2 x = n H 2 S O 4 = 0 , 405 ⇒ n A l = 0 , 1 x = 0 , 2025 n F e = 0 , 135 n A l 2 O 3 / Y = 0 , 06 ⇒ m A l / X = 27 0 , 1 + 0 , 06 . 2 = 5 , 92 g a m n F e n O = 0 , 135 0 , 06 . 3 = 3 4 ⇒ F e 3 O 4

Đáp án : D
Vì các phản ứng hoàn toàn
Y + NaOH có H2 => Al dư
=> nAl dư = 2 3 n H 2 = 0,1 mol
=> Oxit chuyển hết thành Fe
n H 2 S O 4 = 0,405 mol => nFe = 0,135 mol
Y gồm 0,1 mol Al ; Al2O3 và 0,135 mol Fe
=> n A l 2 O 3 = 0,06 mol
Bảo toàn Al : nAl bđ = nAl dư + 2 n A l 2 O 3 = 0,22 mol
=> mAl bđ = 5,94g
Ta có : nFe : nO = 0,135 : 0,18 = 3 : 4
=> Oxit là Fe3O4

\(n_{Cl_2}=\dfrac{0,99.3,7185}{0,082.\left(273+25\right)}=0,15\left(mol\right)\)
PTHH: 2Fe + 3Cl2 --to--> 2FeCl3
__________0,15-------->0,1________(mol)
=> \(C_{M\left(FeCl_3\right)}=\dfrac{0,1}{0,5}=0,2M\)


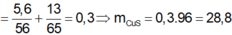
2Fe+3Cl2-to>2FeCl3
0,05---------------0,05
nFe=2,8\56=0,05 mol
=>mFeCl3=0,05.162,5=8,125g