Hòa tan hết m gam hỗn hợp AL và Fe trong dd H2SO4 loãng thoát ra 0,4 mol khí còn trong dư dd NaOh thì thu được 0,3 mol khí Gia trị của m là
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Những câu hỏi liên quan

3 tháng 4 2018
Đáp án B
Đặt nFe = a và nAl = b bảo toàn e ta có:
2a + 3b = 0,4×2 || 3b = 0,3×2 ||⇒ nFe = 0,1 và nAl = 0,2.
⇒ m = 0,1×56 + 0,2×27 = 11 gam

21 tháng 10 2018
Đặt nFe = a và nAl = b bảo toàn e ta có:
2a + 3b = 0,4×2
3b = 0,3×2
⇒ nFe = 0,1 và nAl = 0,2.
⇒ m = 0,1×56 + 0,2×27 = 11 gam
Đáp án B

26 tháng 7 2023
Y tác dụng NaOH cho khí hydrogen nên Y có Al dư.
\(2Al+Fe_2O_3-t^0>Al_2O_3+2Fe\\ Y:Al_{dư}\left(a\left(mol\right)\right),Fe\left(2b\left(mol\right)\right),Al_2O_3\left(b\left(mol\right)\right)\\ n_{H_2}=\dfrac{3}{2}a+2b=0,4\\ n_{Al\left(dư\right)}=\dfrac{2}{3}n_{H_2}=0,2mol=a\\ b=0,05mol\\ BTKL:m=27a+56\cdot2b+102b=16,1g\)

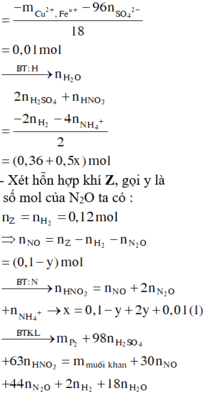


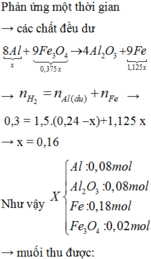
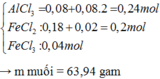
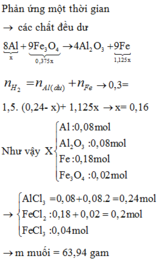
Đặt x- n Fe ; y- n Al
Hỗn hợp + H2SO4 loãng
Fe----> Fe2+ + 2e
x---------------->2x
Al----> Al3+ + 3e
y---------------->3y
2H+ + 2e----> H2
...........0,8<----0,4
Bảo toàn e: 2x+3y=0,8 (1)
Hỗn hợp + NaOH dư
Al----> Al3+ + 3e
y---------------->3y
2H+ + 2e----> H2
...........0,6<----0,3
Bảo toàn e =>3y=0,6 (2)
Từ (1), (2) => x= 0,1 ; y=0,2
=> m= 0,1.56+0,2.27=11 (g)
Khi tác dụng với NaOH chỉ có Al tác dụng tạo khí
2Al + 2NaOH +2H2O => 2NaAlO2 + 3H2
0,2 ---------------------------------------- 0,3
Khi tác dụng với H2SO4 loãng thì cả hai đều phản ứng
2Al + 3H2SO4 => Al2(SO4)3 + 3H2
0,2--------------------------------------- 0,3
Fe + H2SO4 => FeSO4 +H2
0,1--------------------------- 0,1
=> m= 0,2.27+0,1.56=5,4+5,6=11 g