CÂU 1 : Người ta sản xuất axit sunfuric theo sơ đồ sau Fes2 ➝ So2 ➝So3 ➝ H2So4 tính lượng H2So4 sản xuất được từ 240 kg hoặc FeS biết hiệu suất của cả quá trình là 85%
Câu 2: Sau khi hào tan 8,45g oleum A vào nước được dung dịch B, để trung hoà dung dịch B cần 200ml dung dịch nạp 1M . Xác định công thức của A
Mong anh chị giúp đỡ em ạ !!

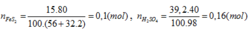

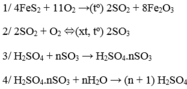
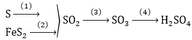


Câu 1:
\(4FeS_2+11O_2\rightarrow2Fe_2O_3+8SO_2\)
\(2SO_2+O_2\rightarrow2SO_3\)
\(SO_3+H_2O\rightarrow H_2SO_4\)
\(n_{SO2}=2n_{FeS2}=\frac{240}{120}.2=4\left(mol\right)\)
\(n_{SO3}=n_{SO2}=4\left(mol\right)\)
\(n_{H2SO4}=n_{SO3}=4\left(mol\right)\)
\(\Rightarrow m_{H2SO4}=98.4=392\left(kg\right)\)
Câu 2:
\(H_2SO_4.nSO_3+nH_2O\rightarrow\left(n+1\right)H_2SO_4\)
\(\frac{8,45}{98+80n}\) ________________________\(0,1\)__(mol)
\(H_2SO_4+2NaOH\rightarrow Na_2SO_4+2H_2O\)
0,1_________0,2_______________
\(\Rightarrow\frac{8,45\left(n+1\right)}{98+80n}=0,1\Rightarrow n=3\)
Vậy oleum A là H2SO3.38O3