Bài bài tập bảo toàn e
Bài 1: cho 3,84 gam Cu tác dụng với 80 ml dung dịch hỗn hợp gồm HNO3 1Mvà HCl 1M sẽ thu được tối đa bao nhiêu lít NO (dktc)
Bài 2: So sánh thể tích khí NO duy nhất thoát ra trong 2 thí nghiệm sau
a) cho 6,4 gam Cu tác dụng với 120 ml dung dịch HNO3 1M
b) cho 6,4 g Cu tác dụng với 120 ml dung dịch hỗn hợp HNO3 1M và H2 SO4 0,5M. Cô cạn dung dịch ở trường hợp b sẽ thu được bao nhiêu gam muối khan (giả thiết các phản ứng xảy ra hoàn toàn các khí đo ở cùng điều kiện)
Bài 3 Hòa tan hoàn toàn 1,62 g Al trong 280 ml dung dịch HNO3 1M thu được dung dịch A và khí NO (là sản phẩm khử duy nhất).Mặt khác cho 7,35 g hai kim loại kiềm thuộc hai chu kì liên tiếp vào 500 ml dung dịch HCl được dung dịch B và 2,8 lít H2 (dktc) .Khi trộn dung dịch A và dung dịch B Thấy tạo thành 1,56 gam kết tủa. Xác định tên hai kim loại và tính nồng độ mol của dung dịch HCl đã dùng

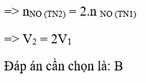

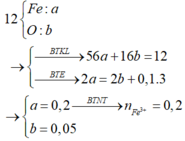
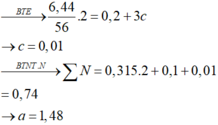
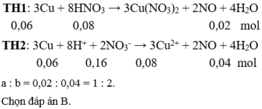
Câu 1:
\(\left\{{}\begin{matrix}n_{Cu}=0,06\left(mol\right)\\n_{HNO3}=0,08\left(mol\right)\\n_{HCl}=0,08\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{H^+}=n_{HNO3}+n_{HCl}=0,16\left(mol\right)\)
\(n_{NO3^-}=n_{HNO3}=0,08\left(mol\right)\)
PTHH :
\(3Cu+8H^++2NO^-_3\rightarrow3Cu^{2+}+2NO+4H_2O\)
Theo PT , đề bài ta thấy Cu và H+ hết NO3− dư
\(\Rightarrow n_{NO}=\frac{2}{3}n_{Cu}=0,06.\frac{2}{3}=0,04\left(mol\right)\)
\(\Rightarrow V_{NO}=0,04.22,4=0,896\left(l\right)\)