Cho 2,24 lít H2 tác dụng với 3,36 lít Cl2 thu được khí X. Cho X tác dụng với dung dịch AgNO3 dư thu được 11,48gam kết tủa trắng. Tính hiệu suất của phản ứng ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{AgCl}=\dfrac{43.05}{143.5}=0.3\left(mol\right)\) \(\Rightarrow n_{HCl}=0.3\left(mol\right)\)
\(n_{HCl}=\dfrac{6.72}{22.4}=0.3\left(mol\right),n_{Cl_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(H_2+Cl_2\underrightarrow{^{^{t^0}}}2HCl\)
\(0.15....0.15.......0.3\)
\(H\%=\dfrac{0.15}{0.2}\cdot100\%=75\%\)

nAgCl = 0.08 mol => nHCl = 0.08 mol
nH2 = 0.1 mol
nCl2 = 0.15 mol
H2 + Cl2 -to-> 2HCl
0.04__________0.08
H% = 0.04/0.1 * 100% = 40%
Tính theo H2 vì Cl2 phản ứng dư
n AgCl=11,48/143,5=0,08(mol)
H2+Cl2---->2HCl(1)
AgNO3+HCl--->AgCl+HNO3(2)
n H2=2,24/22,4=0,1(mol)
n Cl2=3,36/22,4=0,15(mol)
--->Cl2 dư------>khí sau pư gồm cl2 và HCl
n HCl dư=0,15-0,1=0,05(mol)
3Cl2+A5gNO3+3H2O--->5AgCl+5HNO3+HClO3(3)
Theo pthh1
n HCl = 2n H2 = 0,2(mol)
Theo pthh2
n AgCl=n HCl=0,2(mol)
Theo pthh3
n AgCl=5/3n Cl2=0,0833(mol)
\(\sum n_{AgCl}\) tính được =0,0833+0,2=0,2833(mol)
H%=0,08/0,2833.100%=28,24%
Chúc bạn học tốt

\(n_{H_2}=\dfrac{1}{22,4}=\dfrac{5}{112}\left(mol\right)\)
\(n_{Cl_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
PTHH: H2 + Cl2 --as--> 2HCl
Xét tỉ lệ: \(\dfrac{\dfrac{5}{112}}{1}>\dfrac{0,03}{1}\) => Hiệu suất tính theo Cl2
\(n_{AgCl}=\dfrac{7,175}{143,5}=0,05\left(mol\right)\)
Bảo toàn Cl: \(n_{Cl_2\left(pư\right)}=0,025\left(mol\right)\)
\(H\%=\dfrac{0,025}{0,03}.100\%=83,33\%\)

\(n_{AgCl}=\dfrac{7,175}{143,5}=0,05\left(mol\right)\)
PTHH: HCl + AgNO3 ---> AgCl↓ + HNO3
0,05<---------------0,05
\(\rightarrow m_{HCl}=0,05.36,5=1,825\left(g\right)\\
\rightarrow C\%_{ddA}=\dfrac{1,825}{50}.100\%=3,65\%\)
\(n_{Cl_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Đặt H = x%
PTHH: Cl2 + H2 --as--> 2HCl
LTL: 6,72 < 10 => H2 dư
=> nHCl = 0,3x (mol)
\(\rightarrow C\%_{HCl}=\dfrac{0,3x.36,5}{0,3x.36,5+385,4}.100\%=3,65\%\\ \Leftrightarrow20,23\%\)
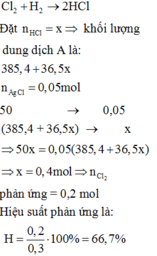




\(PTHH:H_2+Cl_2\rightarrow2HCl\left(1\right)\)
\(HCl+AgNO_3\rightarrow AgCl+HNO_3\left(2\right)\)
Ta có :
\(n_{H2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
\(n_{Cl2}=\frac{3,36}{22,4}=0,15\left(mol\right)\)
Theo PTHH: (1)
\(\Rightarrow\frac{0,1}{1}< \frac{0,15}{1}\) nên sau phản ứng H2 hết, Cl2 dư
\(\Rightarrow n_{HCl}=2n_{H2}=0,2\left(mol\right)\)
Theo PTHH (2) \(\Rightarrow n_{AgCl}=0,2\left(mol\right)\)
\(\Rightarrow m_{AgCl}=0,2.143,5=28,7\%\)
\(\Rightarrow H=\frac{11,48}{28,7}.100\%=40\%\)