Đốt cháy 3,36 lít hỗn hợp 2 hydrocacbon X,Y thu được 8,96 lít CO2 và 7,2g H2O a/ tìm công thức phân tử của X,Y b/ tính % số mol của mỗi hidrocacbon
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án C
Khí thoát ra khỏi bình là Y ; nCO2 = 0,03 ; nH2O= 0,04
→ Y là ankan → nY = 0,04 - 0,03 = 0,01 → Y là C3H8
Đốt cháy X thu được nCO2 = nH2O
→ nC2H2= nC3H8 = 0,01 mol
→ nC2H4 = ( 0,82 - 0,01 × 26 ) : 28 = 0,02 mol
→ nX = 0,01 + 0,02 + 0,01 = 0,04 → VX = 0,896 (l)

Đáp án D
nCO2= 25/328mol
nH2O=21/328mol
=> nCO2 > nH2O
Dễ thấy đốt X thu được nCO2 < nH2O
=> Đốt Y phải thu được nCO2 > nH2O
=> X là ankan

Khí thoát ra khỏi bình là Y; n(CO2) = 0,03 mol; n(H2O) = 0,04 mol
→ Y là ankan → n(Y) = 0,01 → Y là C3H8
Đốt cháy X thu được n(CO2) = n(H2O) → n(C2H2) = n(C3H8) = 0,01 mol
→ n(C2H4) = (0,82 – 0,01*26)/28 = 0,02 mol
→ n(X) = 0,01 + 0,02 + 0,01 = 0,04 → V(X) = 0,896 lít → Đáp án C


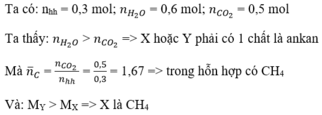
a, \(n_{CO2}=\frac{8,96}{22,4}=0,4\left(mol\right)\)
\(n_{H2O}=\frac{7,2}{18}=0,4\left(mol\right)\)
\(\Rightarrow X,Y:Anken\)
\(\Rightarrow C=\frac{0,4}{0,15}=2,67\)
Vậy X là C2H4 , Y là C3H6
b,
\(hh:C_2H_4:a\left(mol\right):C_3H_6:b\left(mol\right)\)
Giải hệ PT:
\(\left\{{}\begin{matrix}a+b=0,15\\2a+3b=0,4\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,05\\b=0,1\end{matrix}\right.\)
\(\Rightarrow\%_{C2H4}=33,33\%\Rightarrow\%C_3H_6=66,67\%\)