C1
Đốt cháy hoàn toàn m gam khí A thu đc 6,6 gam khí cacbonic và 2,7 gam nước. Ở cùng điều kiện nhiệt độ và áp suất 3,7 gam khí A có thể tích bằng thể tích của 1,6 gam oxi. Biết nguyên tử A có chứa 2 nguyên tử oxi. Tính m và tìm công thức phân tử của A
C2
Đốt cháy hoàn toàn 10,4 gam hợp chất hữu cơ A rồi cho sản phẩm lần lượt qua bình 1 đựng h2so4 đậm đặc,bình 2 chứa nước vôi trong dư, thấy khối lượng bình 1 tăng 3,6 gam ở bình 2 thu đc 30gam kết tủa. Khi hoá hơi 5,2 gam A thu đc một thể tích bằng thể tích của 1,6 gam oxi ở cùng điều kiện nhiệt độ và áp suất. Xác định CTPT của A

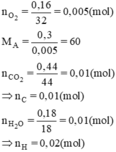
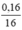 = 0,01(mol)
= 0,01(mol)
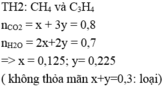
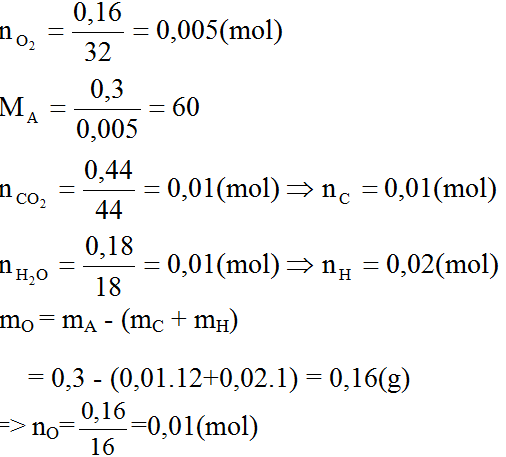
Câu 1 :
A có dạng CxHyO2.
\(n_A=n_{O2}=\frac{1,6}{16.2}=0,05\left(mol\right)\)
\(\Rightarrow M_A=\frac{3,7}{0,05}=74\Rightarrow12x+y+32=74\)
\(C_xH_yO_2+\left(x+\frac{y}{4}-1\right)O_2\rightarrow xCO_2+\frac{y}{2}H_2O\)
Ta có:
\(n_{CO2}=\frac{6,6}{44}=0,15\left(mol\right);n_{H2O}=\frac{2,7}{18}=0,15\left(mol\right)\)
\(\Rightarrow x:y=n_{CO2}:2n_{H2O}=1:2\)
Vậy x = 3; y = 6 suy ra A là C3H6O2.
\(\Rightarrow m=\frac{0,15}{3}.74=3,7\left(g\right)\)
Câu 2 :
Ta có :
\(n_A=n_{O2}=\frac{1,6}{16.2}=0,05\left(mol\right)\Rightarrow M_A=\frac{5,2}{0,05}=104\)
\(\Rightarrow n_A=\frac{10,4}{104}=0,1\left(mol\right)\)
A có dạng CxHyOz \(\Rightarrow12x+y+16z=104\)
Đốt A
\(C_xH_yO_z+\left(x+\frac{y}{4}-\frac{z}{2}\right)O_2\rightarrow xCO_2+\frac{y}{2}H_2O\)
Sản phẩm cháy gồm CO2 và H2O, dẫn qua bình 1 thì H2O bị hấp thu
\(n_{H2O}=\frac{3,6}{18}=0,2\left(mol\right)\)
\(\Rightarrow y=\frac{n_{H2O}}{n_A}=\frac{0,2.2}{0,1}=4\)
Dẫn qua bình 2 thì CO2 phản ứng
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
\(n_{CaCO3}=n_{CO2}=\frac{30}{100}=0,3\left(mol\right)\)
\(\Rightarrow x=\frac{n_{CO2}}{n_A}=\frac{0,3}{0,1}=3\)
Thay vào giải được z = 4 vậy A là C3H4O4