Để điều chế 3,36l O2 phải dùng hết 40,4g KMnO3.Tính
a) H%?
b) % về m mỗi chất trong hỗn hợp chất rắn còn lại sau quas trình nhiệt phân
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a)n_{KMnO_4} = a; n_{KClO_3} = b\Rightarrow 158a + 122,5b = 99,95(1)\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ 2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2\\ n_{O_2} = 0,5a +1,5b = \dfrac{14,56}{22,4}=0,65(2)\\ (1)(2)\Rightarrow a = 0,4 ; b = 0,3\\ \%m_{KMnO_4} = \dfrac{0,4.158}{99,95}.100\% = 63,23\%\\ \%m_{KClO_3} = 100\%-63,23\% = 36,77\%\)
\(n_{K_2MnO_4} = n_{MnO_2} = 0,5a = 0,2(mol)\\ n_{KClO_3} = b = 0,3(mol)\\ m_{hh\ sau\ pư} = 99,95 - 0,65.32 = 79,15(gam)\\ \%m_{K_2MnO_4} = \dfrac{0,2.197}{79,15}.100\% = 49,78\%\\ \%m_{MnO_2} = \dfrac{0,2.87}{79,15},100\% = 21,98\%\\ \%m_{KCl} = 28,24\%\)

mgiảm = mO (sinh ra) = 100 - 90,4 = 9,6 (g)
-> nO2 = \(\dfrac{9,6}{32}=0,3\left(mol\right)\)
PTHH: 2KClO3 \(\underrightarrow{t^o,MnO_2}\) 2KCl + 3O2
0,2 0,6
mKCl = 0,2.74,5 = 19,9 (g)
mKClO3 = 90,4 - 19,9 = 70,5 (g)

\(2NaHCO_3-^{t^o}\rightarrow Na_2CO_3+CO_2+H_2O\\ n_{CO_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\\ n_{NaHCO_3}=2n_{CO_2}=0,1\left(mol\right)\\ \%m_{NaHCO_3}=\dfrac{0,1.84}{19}.100=44,21\%\\ \%m_{Na_2CO_3}=55,79\%\\ ChấtrắnC:Na_2CO_3\\ m_{Na_2CO_3\left(bđ\right)}=19-8,4=10,6\left(g\right)\\ n_{Na_2CO_3\left(sinhra\right)}=n_{CO_2}=0,05\left(mol\right)\\ \Rightarrow m_{ChấtrắnC}=m_{Na_2CO_3\left(bđ\right)}+m_{Na_2CO_3\left(sinhra\right)}=10,6+0,05.106=15,9\left(g\right)\)

a) \(n_{SO_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH: S + O2 --to--> SO2
0,5<-0,5<------0,5
=> mS = 0,5.32 = 16(g)
=> \(\left\{{}\begin{matrix}\%m_S=\dfrac{16}{22,2}.100\%=72,07\%\\\%m_P=\dfrac{22,2-16}{22,2}.100\%=27,93\%\end{matrix}\right.\)
b) \(n_P=\dfrac{22,2-16}{31}=0,2\left(mol\right)\)
PTHH: 4P + 5O2 --to--> 2P2O5
0,2-->0,25----->0,1
=> \(V_{O_2}=0,25.22,4=5,6\left(l\right)\)
c)
PTHH: 2KClO3 --to--> 2KCl + 3O2
0,5<-------------------0,75
=> \(m_{KClO_3}=0,5.122,5=61,25\left(g\right)\)
a) PTHH:
\(S+O_2\rightarrow\left(t^o\right)SO_2\\ 4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\)
- Chất khí mùi hắc là SO2
- Chất rắn sau phản ứng có m(g) là P2O5
Đặt: nS=a(mol); nP=b(mol) (a,b>0) (nguyên, dương)
\(\Rightarrow\left\{{}\begin{matrix}32a+31b=22,2\\22,4a=11,2\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,5\\b=0,2\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}\%m_S=\dfrac{0,5.32}{22,2}.100\approx72,072\%\\\%m_P\approx100\%-72,072\%\approx27,928\%\end{matrix}\right.\)
b)
\(n_{O_2}=a+\dfrac{5}{4}b=0,5+\dfrac{5}{4}.0,2=0,75\left(mol\right)\\ \Rightarrow V_{O_2\left(đktc\right)}=0,75.22,4=16,8\left(l\right)\)
c)
\(2KClO_3\rightarrow\left(t^o\right)2KCl+3O_2\\ n_{KClO_3}=\dfrac{2}{3}.n_{O_2}=\dfrac{2.0,75}{3}=0,5\left(mol\right)\\ \Rightarrow m_{KClO_3}=122,5.0,5=61,25\left(g\right)\)

a)
$4P + 5O_2 \xrightarrow{t^o} 2P_2O_5$
$S + O_2 \xrightarrow{t^o} SO_2$
b) Gọi $n_P = a(mol) ; n_S = b(mol) \Rightarrow 31a + 32b = 15,6(1)$
Theo PTHH :
$n_{O_2} = \dfrac{5}{4}n_P + n_S = \dfrac{5a}{4} + b = \dfrac{13,44}{22,4} = 0,6(2)$
Từ (1)(2) suy ra : a = 0,4 ; b = 0,1
$m_P = 0,4.31 = 12,4(gam)$
$m_S = 0,1.32 = 3,2(gam)$
c) $n_{P_2O_5} = \dfrac{1}{2}n_P = 0,2(mol) \Rightarrow m_{P_2O_5} = 0,2.142 = 28,4(gam)$
$n_{SO_2} = n_S = 0,1(mol) \Rightarrow V_{SO_2} = 0,1.22,4 = 2,24(lít)$

PTHH:
\(CaCO_3+2HCl\rightarrow CaCl_2+H_2O+CO_2\uparrow\)
0,15 0,15
\(CaO+2HCl\rightarrow CaCl_2+H_2O\)
Ta có: \(n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(\Rightarrow m_{CaCO_3}=0,15\cdot100=15\left(g\right)\)
\(\Rightarrow m_{CaO}=20,6-15=5,6\left(g\right)\)
\(\Rightarrow\%m_{CaCO_3}=\dfrac{15\cdot100}{20,6}\approx73\%\)
\(\Rightarrow\%m_{CaO}=100\%-73\%=27\%\)

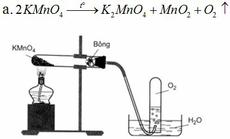
b.
Rắn A gồm: KMnO4, K2MnO4, MnO2
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 ↑+ 8H2O
K2MnO4 + 8HCl → 2KCl + MnCl2 + 2Cl2↑ + 4H2O
MnO2 + 4HCl → MnCl2 + Cl2↑ + 2H2O
Vậy khí B là Cl2.
a)2 KMnO4------->K2MnO4+MnO2+O2
n O2=3,36/22,4=0,15(mol)
Theo pthh
n KMnO4=2n O2=0,3(mol)
m KMnO4=0,3.158=47,4(g)
H%=40,4/47,4.100%=85,23%
b) n K2MnO4=n MnO2=n O2=0,15(mol)
m K2MnO4=0,15.197=29,55(g)
m MnO2=87.0,15=13,05(g)
m hh=29,55+13,05=42,6(g)
%m K2MnO4=29,55/42,6.100%=69,37%
%m MnO2=100-69,37=30,63%
Chúc bạn học tốt