Cho 9,12 g hỗn hợp gồm FeO , Fe2O3 , Fe3O4 tác dụng với dd HCl dư . Sau phản ứng xảy ra hoàn toàn , được dd Y ; cô cạn dd Y thu được 7,62 g FeCl2 và m (g) FeCl3 . Tính m ?
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Những câu hỏi liên quan

MN
6 tháng 2 2021
FeO + 2HCl => FeCl2 + H2O
Fe2O3 + 6HCl => 2FeCl3 + 3H2O
Quy đổi hỗn hợp chỉ gồm : FeO , Fe2O3
nFeCl2 = 7.62/127 = 0.06 (mol)
=> nFeO = nFeCl2 = 0.06 (mol)
mFeO = 0.06*72 = 4.32 (g)
mFe2O3 = 9.12 - 4.32 = 4.8 (g)
nFe2O3 = 4.8/160 = 0.03 (mol)
nFeCl3 = 2nFe2O3 = 0.06 (mol)
mFeCl3 = 0.06*162.5 = 9.75 (g)

26 tháng 1 2022
Quy đổi Fe3O4 thành FeO, Fe2O3
\(n_{FeCl_2}=\dfrac{7,62}{127}=0,06\left(mol\right)\)
PTHH: FeO + 2HCl --> FeCl2 + H2O
0,06<------------0,06
=> \(n_{Fe_2O_3}=\dfrac{9,12-0,06.72}{160}=0,03\left(mol\right)\)
PTHH: Fe2O3 + 6HCl --> 2FeCl3 + 3H2O
0,03-------------->0,06
=> \(m_{FeCl_3}=0,06.162,5=9,75\left(g\right)\)


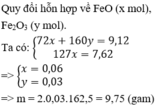

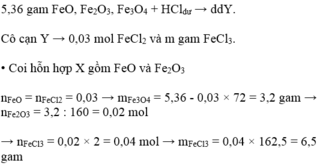
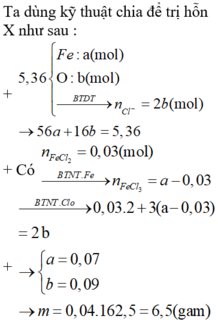
Ta có
Coi như trong hỗn hơp chỉ gồm FeO (a)và Fe2O3(b)
Ta có nFeCl2=\(\frac{6,72}{127}\)=0,06(mol)
\(\rightarrow\)nFeO=0,06(mol)
mFeO+mFe2O3=9,12\(\rightarrow\)mFe2O3=4,8(g)
\(\rightarrow\) nfe2O3=\(\frac{4,8}{160}\)=0,03(mol)
\(\rightarrow\)nFecl3=2nFe2O3=0,03.2=0,06(mol)
m=0,06.162,5=9,75(g)