Một hỗn hợp X gồm 2 kim loại A, B thuộc 2 chu kì liên tiếp trong bảng tuần hoàn, có khối lượng là 8,5g. Cho X phản ứng hết với nước cho ra 3,36 lít khí H2 (đktc).
a, Xác định 2 kim loại và tính khối lượng mỗi kim loại trong hỗn hợp ban đầu.
b, Thêm vào 8,5g hỗn hợp X trên, 1 kim loại kiềm thổ D được hỗn hợp Y, cho Y tác dụng với nước thu được dung dịch E và 4,48 lít khí H2 ( đktc). Cô cạn dung dịch E ta được chất rắn Z có khối lượng là 22,15g. Xác định D và khối lượng của D.


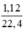 = 0,05(mol)
= 0,05(mol)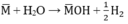
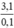 = 31 → Na, K
= 31 → Na, K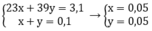
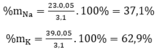
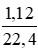 = 0,05(mol)
= 0,05(mol)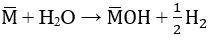
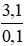 = 31 → Na, K
= 31 → Na, K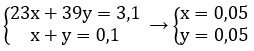
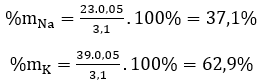
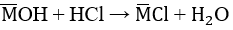
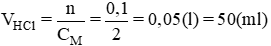
a)
2X+2H2O\(\rightarrow\)2XOH+H2
nH2=\(\frac{3,36}{22,4}\)=0,15(mol)
\(\rightarrow\)MX=\(\frac{8,5}{0,3}\)=28,333(g)
\(\rightarrow\)2 kim loại là Na và K
Ta có hh gồm Na(a mol) K (b mol)
Ta có \(\left\{{}\begin{matrix}\text{23a+39b=8,5}\\\text{a+b=0,3}\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}\text{a=0,2 }\\\text{b=0,1}\end{matrix}\right.\)
\(\text{mNa=0,2.23=4,6(g)}\)
\(\text{mK=0,1.39=3,9(g)}\)
b)
D+2H2O\(\rightarrow\)D(OH)2+H2(1)
Ta có nH2=4,48/22,4=0,2(mol)
\(\rightarrow\)nH2(1)=0,05(mol)
Ta có mNaOH+mKOH+mD(OH)2=22,15
\(\rightarrow\)mD(OH)2=8,55(g)
\(\rightarrow\)MD(OH)2=171(đVC)
\(\rightarrow\)MD=137
\(\rightarrow\)D là Ba
\(\text{mBa=0,05.137=6,85(g)}\)