Trộn 100 ml NaOH 1M với 100ml HCl 1M cùng nhiệt độ 24, 6o C trong 1 nhiệt luownh kế đoạn nhiệt; sau phản ứng thấy nhiệt độ cỉa hệ đạt 31,3o C. Tính hiệt ứng nhiệt phản ứng trung hòa.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Thí nghiệm 1:
2HCl + MgO → MgCl2 + H2O
=> Cốc thí nghiệm nguội dần ( HCl ban đầu hơi ấm) => Phản ứng thu nhiệt.
Thí nghiệm 2:
CH3COOH + NaHCO3 → CH3COONa + CO2 + H2O
=> Cốc thí nghiệm nóng lên => Phản ứng tỏa nhiệt.

1.
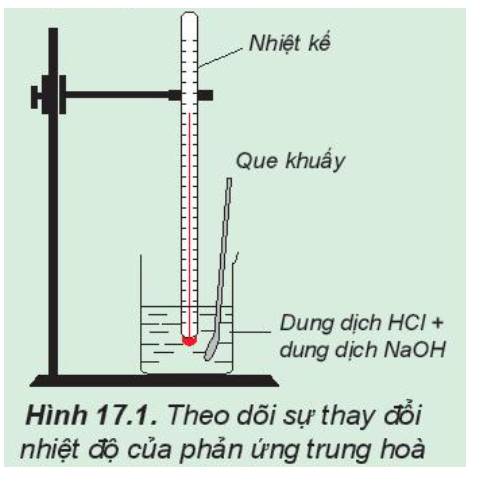
Phản ứng hóa học: NaOH + HCl → NaCl + H2O
Nhiệt độ đo được (HCl) lúc ban đầu thấp hơn so với nhiệt độ sau phản ứng
=> Phản ứng trung hòa là phản ứng tỏa nhiệt
2.
Trong thí nghiệm trên, nếu thay các dung dịch HCl và NaOH bằng các dung dịch loãng hơn thì nhiệt độ sau phản ứng vẫn tăng nhưng tăng ít hơn so với thí nghiệm trên.

a)nHCl= 0,1 , nNaOh=0,4 khi phân li ra ta thu được các ion; H+, Cl- Na+, OH- Vdung dịch sau = 0,1+0,4=0,5(l)
nH+=nCl-=0,1 [H+]=[Cl-]=0,1/0,5=0,2 (M)
nNa+=nOH-=0,4 [Na+]=[OH-]=0,4/0,5=0,8
b)nH+=0,1 nOH-=0,4 --> OH- dư --> nOHdư=0,4-0,1=0,3 --> [OHdư ]=0,3/0,5=0,6 --> pOh=0,23--> ph=14-0,23=13,77

\(n_{HCl}=0.1\cdot0.03=0.003\left(mol\right)\)
\(n_{NaOH}=0.1\cdot0.01=0.001\left(mol\right)\)
\(NaOH+HCl\rightarrow NaCl+H_2O\)
Lập tỉ lệ :
\(\dfrac{0.003}{1}>\dfrac{0.001}{1}\Rightarrow HCldư\)
\(n_{HCl\left(dư\right)}=0.003-0.001=0.002\left(mol\right)\)
\(\left[H^+\right]=\dfrac{0.002}{0.1+0.1}=0.01\)
\(pH=-log\left(0.01\right)=2\)
\(b.\)
\(Ba\left(OH\right)_2+2HCl\rightarrow BaCl_2+2H_2O\)
\(0.001..........0.002\)
\(V_{Ba\left(OH\right)_2}=\dfrac{0.001}{1}=0.001\left(l\right)\)

Ok, để thử coi chứ tui ngu hóa thấy mồ :(
a/ \(n_{NaOH}=0,2.0,1=0,02\left(mol\right)\)
\(NaOH\rightarrow Na^++OH^-\)
\(n_{Na^+}=n_{OH^-}=0,02\left(mol\right)\)
\(\Rightarrow C_{MNa^+}=\frac{0,02}{0,4+0,1}=0,04\left(mol/l\right)\)
\(n_{Ba\left(OH\right)_2}=0,3.0,4=0,12\left(mol\right)\)
\(Ba\left(OH\right)_2=Ba^{2+}+2OH^-\)
\(\Rightarrow n_{OH^-}=0,24\left(mol\right);n_{Ba^{2+}}=0,12\left(mol\right)\)
\(\Rightarrow C_{MBa^{2+}}=\frac{0,12}{0,5}=0,24\left(mol/l\right)\)
\(n_{OH^-}=0,02+0,24=0,26\left(mol\right)\)
\(\Rightarrow C_{MOH^-}=\frac{0,26}{0,5}=0,52\left(mol/l\right)\)
b/ \(n_{HCl}=0,2V\left(mol\right)\)
\(\Rightarrow n_{H^+}=n_{Cl^-}=0,2V\)
\(\Rightarrow C_{MCl^-}=\frac{0,2V}{2V}=0,1\left(mol/l\right)\)
\(n_{H_2SO_4}=0,3V\left(mol\right)=\frac{n_{H^+}}{2}=n_{SO_4^{2-}}\)
\(\Rightarrow C_{MSO_4^{2-}}=\frac{0,3V}{2V}=0,15\left(mol/l\right)\)
\(n_{H^+}=0,2V+0,6V=0,8V\left(mol\right)\)
\(\Rightarrow C_{MH^+}=\frac{0,8V}{2V}=0,4\left(mol/l\right)\)
Bác nào hảo tâm giúp em mấy câu còn lại chớ đến đây thì em chịu chết òi :(



Đề có thiếu j không