Trộn 24 gam Fe2O3 với 10,8 gam Al rồi nung ở nhiệt độ cao, hỗn hợp sau phản ứng hòa tan vào dung dịch NaOH dư thu được 5,376 lít khí ( đktc). Tính hiệu suất của phản ứng nhiệt nhôm.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Giải thích:
nAl = 0,4 mol ; nFe3O4 = 0,15 mol
Giả sử H = x
![]()
Bd: 0,4 0,15
Pu: 0,4x 0,15x 0,2x 0,45x
Sau: 0,4 – 0,4x 0,45x
nH2 = 1,5nAl + nFe → 0,48 = 1,5(0,4 – 0,4x) + 0,45x
→ x = 0,8
→ H = 80%
Đáp án D

2Al + F e 2 O 3 → A l 2 O 3 + 2Fe
Sau phản ứng cho hỗn hợp rắn tác dụng với dd NaOH thấy có khí thoát ra, suy ra có Al dư.
Vậy hỗn hợp rắn: Fe, A l 2 O 3 , Al (dư) và F e 2 O 3 (nếu dư).
Theo định luật bảo toàn khối lượng, ta có:
m X = m r ắ n tan + m r ắ n k h ô n g tan
= 21,67 - 12,4 = 9,27g
Mà m r ắ n tan = m A l d u + m A l 2 O 3
2Al + 2NaOH + 2 H 2 O
→ 2 N a A l O 2 + 3 H 2 1
Theo PTHH (1), ta có:
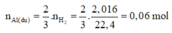
⇒ m A l d u = 0,06.27 = 1,62g
⇒ m A l 2 O 3 p u = m r a n tan - m A l d u
= 9,27-1,62=7,65 g
⇒ n A l 2 O 3 p u = 0,075mol
⇒ n A l p u = n F e s p = 2 n A l 2 O 3 p u
= 0,075.2 = 0,15 mol
Ta có:
m ran khong tan = mFe (sp) = mFe2O3(neu dư)
⇒ m F e 2 O 3 (neu dư)=12,4-0,15.56 = 4g
⇒ n F e 2 O 3 dư = 4/160 = 0,025 mol
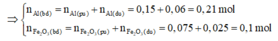
Giả sử phản ứng hoàn toàn thì Al sẽ dư → Tính hiệu suất phản ứng nhiệt nhôm theo F e 2 O 3 .
⇒ H = 0,075.100/0,1 = 75%
⇒ Chọn D.

Gọi nAl=x mol và nFe2O3 = y mol
Fe2O3 + 2Al → Al2O3 + 2Fe
Đầu(mol) y x
Do chất rắn sau +NaOH tạo khí nên dư Al
=> nH2=1,5nAl => 0,06= x-a mX= 160y + 27x = 21,67
m rắn không tan = mFe2O3 + mFe = 160(y – ½ a) + 56a=12,4
Giải hệ : x=0,21mol ; y=0,1mol ; a =0,15mol.
Tính hiệu suất theo Fe2O3 => %H= (0,075/0,1) .100%= 75%
=>D

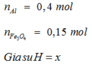
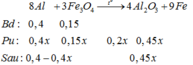
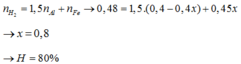

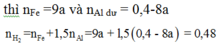
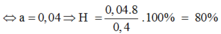
n Al = 0,4 mol, n fe2o3 = 0,15 mol
\(\text{Fe2O3 +2 Al ---> Al2O3 + Fe2}\)
\(\text{nAl/2 < nFe2O3/1}\)
---> Nếu pứ hoàn toàn thì Fe2O3 hết trc
--> Hiệu suất sẽ tính theo fe2o3
vì pứ ko hoàn toàn, hh sau pứ còn pứ vs NaOH sinh ra H2 --> hh có Al
\(\text{Al + NaOH + H2O ---> NaAlO2 +3/2 H2}\)
\(\text{n H2 = 0,24 mol}\)
--> n Al dư = 0,24:3/2= 0,16 mol
--> n Al pứ vs fe2o3 = 0,4 - 0,16= 0,24 mol
---> n Fe2O3 = 0,24÷2=0,12mol
--> H = 0,12:0,15.100= 80%
Fe2O3+2Al→Al2O3+2Fe
Al+NaOH+H2O→NaAlO2+\(\frac{3}{2}\)H2↑
⇒nH2=0,24 mol, nAl (ban đầu)=\(\frac{10,8}{27}\)= 0,4 mol , ⇒nAl (tham gia p/u)=0,24 (mol) ⇒nFe2O3=0,12 mol
⇒H=\(\frac{0,12}{0,15}\cdot100\%\)=80%