1.dẫn V lít CO2 đktc vào 100 ml dd NaOH x mol/l sau phản ứng thu được dd chứa đồng thời 0.1 mol NaHCO3 và 0.05 mol Na2CO3 tìm V và x
2.Tính nồng độ mol của các dd sau phản ứng khi: +dẫn 2.24 lít khí SO2 đktc qua 200ml dd KOH 2M lấy dư +dẫn 6.72 lít khí SO2 đktc qua 200ml dd NaOH 1M

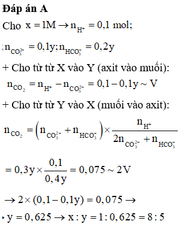
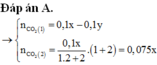
\(\text{1) BT Na ta có nNaOH= n NaHCO3 + 2.nNa2CO3=0,2 mol}\)
--> X= CM NaOH=2M
\(\text{BT C ta có nCO2 = nNaHCO3 + n Na2CO3 =0,15 mol}\)
--> VCO2 =3,36 l
\(\text{2) 0,1 mol CO2 qua 0,4 mol KOH dư }\)
-> dd sau pư là K2SO3=0,1 mol và KOH dư =0,2 mol
-> CM KOH=0,2/0,2 =1M và CM của K2SO3 =0,1/0,2=0,5 M
\(\text{Dẫn 0,3 mol SO2 qua 0,2 mol NaOH}\)
-> tạo ra muối NaHSO3 0,2 mol và 0,1 mol SO2 dư