13) Nung m gam hỗn hợp gồm MgCO3 và CaCO3 đến khối lượng không đổi thì thấy khối lượng chất rắn giảm xuống 49%. Xác định khối lượng các chất có trong hỗn hợp ban đầu
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi khối lượng hỗn hợp ban đầu là 100 g , số mol MgCO3 và CaCO3 lẫn lượt là x và y.
Ta có : 84x+ 100y=100 (g) (1)
PTHH: MgCO3 –to-> MgO + CO2
CaCO3 –to-> CaO + CO2
-> Khối lượng giảm là CO2
-> số mol CO2 là : x+y= 47,5 : 44= 1,08(mol) (2)
Từ (1) và (2) ta suy ra:
x= 0,5(mol)
y= 0,58( mol)
=> % MgCO3 =42%
% CaCO3 = 58%.
Gọi khối lượng hỗn hợp ban đầu là 100 g , số mol MgCO3 và CaCO3 lẫn lượt là x và y.
Ta có : 84x+ 100y=100 (g) (1)
PTHH: MgCO3 ➞ MgO + CO2
CaCO3 ➞ CaO + CO2
-> Khối lượng giảm là CO2
-> số mol CO2 là : x+y= 47,5 : 44= 1,08(mol) (2)
Từ (1) và (2) ta suy ra:
x= 0,5(mol)
y= 0,58( mol)
=> % mMgCO3 =42%
%mCaCO3 = 58%.

Gọi số mol KMnO4, KClO3 là a, b
=> 158a + 122,5b = 49,975
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
_______a----------------------------------->a
2KClO3 --to--> 2KCl + 3O2
_b---------------------->1,5b
mO2 = mgiảm = 10,4
=> \(n_{O_2}=\dfrac{10,4}{32}=0,325\left(mol\right)\)
=> 0,5a + 1,5b = 0,325
=> a = 0,2; b = 0,15
=> \(\left\{{}\begin{matrix}\%KMnO_4=\dfrac{0,2.158}{49,975}.100\%=63,23\%\\\%KClO_3=\dfrac{0,15.122,5}{49,975}.100\%=36,77\%\end{matrix}\right.\)

Gọi $n_{KMnO_4} = a(mol) ; n_{KClO_3} = b(mol) \Rightarrow 158a + 122,5b = 49,975(1)$
$2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2$
$2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2$
$m_{O_2} = m_{giảm} = 4(gam)$
$\Rightarrow n_{O_2} = 0,5a + 1,5b = \dfrac{4}{32} = 0,125(2)$
Từ (1)(2) suy ra a = 0,339 ; b = -0,029 < 0
(Sai đề)

Đáp án A
+ S ơ đ ồ p h ả n ứ n g : C a C O 3 M g O → t 0 ⏟ 30 g a m C a O M g O ⏟ 20 g a m + C O 2 ↑ ⇒ n C a C O 3 = n C O 2 = 30 - 20 44 ⇒ % m C a C O 3 = 10 . 100 44 . 30 = 75 , 76 %

Chọn A
Đề bài chỉ hỏi tỉ lệ giữa các khối lượng nên có thể lấy 90 gam hỗn hợp ban đầu và sau phản ứng còn lại
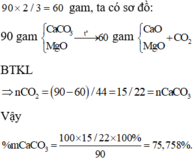

Đáp án A
Định hướng tư duy giải
Giả sử số mol CaCO3 trong hỗn hợp đầu là 1 mol
C a C O 3 → C a O + C O 2 ↑
m t r ư ớ c - m s a u = m C O 2 = m t r ư ớ c - 2 3 m t r ư ớ c
m t r ư ớ c = 3 m C O 2 = 132 g
% m C a C O 3 / h h = 75 , 76 %
