Dẫn luồng khí CO đi qua hỗn hợp gồm CuO và Fe2O3 nung nóng, sau một thời gian thu được chất rắn X và khí Y. Cho Y hấp thụ hoàn toàn vào dung dịch Ba(OH)2 dư, thu được 29,55 gam kết tủa. Chất rắn X phản ứng với dung dịch HNO3 dư thu được V lít khí NO (sản phẩm khử duy nhất, ở đktc). Giá tri của V là ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Ta có sơ đồ phản ứng:
CO + CuO, Fe2O3
→ Chất rắn X chứa Cu, Fe, CuO dư, Fe2O3 dư, FeO, Fe3O4
Khí Y là CO2
CO2+ Ba(OH)2 → BaCO3 ↓ + H2O
Ta có: nCO2= nBaCO3= 29,55/197= 0,15 mol
Chất rắn X + HNO3 → Cu(NO3)2+ Fe(NO3)3
Áp dụng bảo toàn electron cho cả quá trình:
- Quá trình cho electron:
C+2 → C+4+ 2e
0,15 0,15 0,3 mol
- Quá trình nhận electron:
N+5+ 3e →NO
0,3→ 0,1 mol
→ VNO= 22,4. 0,1= 2,24 lít

Đáp án : A
nCO2= nO pứ = nBaCO3 =0,15 mol
Nếu hỗn hợp oxit ban đầu phản ứng với HNO3 thì sẽ không tạo ra sản phẩm khử NO
=> Bảo toàn e : ne KL + CO = ne KL + axit
Mà ne KL + CO = ne O pứ = 2nO = 0,3 mol
=> ne KL + axit = 0,3 mol = 3nNO = > nNO = 0,1 mol
=> VNO = 2,24 lit

Trong trường hợp này, X đã “bão hòa”, không thể cho e được nữa, nhưng nó đã được CO lấy đi một lượng O để phá vỡ trạng thái này. CO + [O] →CO2
Và thế là X trở thành Y, lại có thể cho e với N+5 tạo thành NO, NO2.
Theo lý thuyết, nếu HNO3 lại đưa Y lên trạng thái bão hòa thì số mol e mà N+5 nhận được là 0,24 x 2 = 0,48 mol
Nhưng trên thực tế, con số này là 0,11 x 3 + 0,07 x 1= 0,40 mol
Sở dĩ điều này xảy ra là do có một lượng Fe chỉ tồn tại ở số oxi hóa +2
→ nFe2+ = 0,48 – 0,40 =0,08 → mFe(NO3)2 = 14,4 gam
Chọn đáp án C

\(n_{CO_2}=n_{CO}=\dfrac{p}{100}\left(mol\right)\)
\(\text{Áp dụng định luật bảo toàn khối lượng: }\)
\(m_X+m_{CO}=m_Y+m_{CO_2}\)
\(\Leftrightarrow m_X-m_Y=m_{CO_2}-m_{CO}\)
\(\Leftrightarrow\) \(m-n=\dfrac{p}{100}\cdot44-\dfrac{p}{100}\cdot28=0.16p\)
\(\Leftrightarrow m=n+0.16p\)

Bảo toàn KL ; 24 +mCOp/ư +mCOdu =mY+ mco2 +mCodu Suy ra:: 24+mco(pư) =mY +mCO2 ,,,,,mÀ mol CO(pư)=mol CO2 .ta cần tính mol CO2 là ok.
pt: CO2 + 2OH-→ CO32- ( mol BaCO3: 0,15 ,đặt mol(NaCo3)= amol )\(\Rightarrow\)ΣCo32-=015 +a
(0,15+a) \(\leftarrow\) 0,15+a
CO2+ OH-→ HCO32- (mol Ba(hco3)2=0,05 (bảo toàn Ba2+ ) và mol NaHCO3 =0,2-a → ΣHco32-=0,3-a
0,3-a \(\leftarrow\) 0,3-a
ΣCO2= 0,45mol Lắp vào biểu thức trên tính đk : mY=16,8g

Đáp án : B
nOH = 2nBa(OH)2 + nNaOH = 0,6 mol ; nBa2+ = 0,2 mol > nBaCO3 = 0,15 mol
+) Nếu có sự hòa tan kết tủa : nCO2 = nOH – nCO3 = 0,45 mol
=> m = mX – mO pứ = 24 – 16.0,45 = 3,3g (không có đáp án)
+) Nếu OH dư => nCO2 = nBaCO3 = 0,15 mol
=> m = 21,6g

Đáp án B
nCuO = 0,15mol
nBa(OH)2 = 0,18 mol
n kết tủa = 0,12 mol < nBa(OH)2
=> có 2 trường hợp
Trường hợp 1: CO2 hết, Ba(OH)2 dư
nCO2 = n kết tủa = 0,12 mol
=> nCu = nO tách ra = nCO2 = 0,12 mol => m chất rắn = mAg + mCuO dư = 0,24 . 108 + 0,03 . 80 = 28,32g
Trường hợp 2: Kết tủa bị hòa tan 1 phần
nCO2 = 2nBa(OH)2 – n kết tủa = 2 . 0,18 – 0,15 = 0,21 > nO trong oxit (loại)
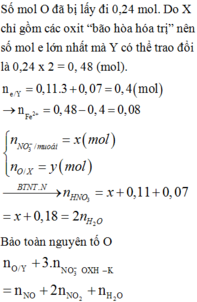
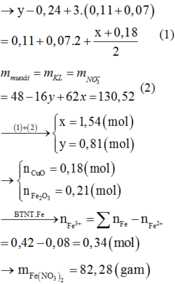
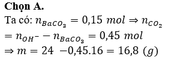
Ba(OH)2 + CO2 ---> BaCO3 +H2O
...................0,15..........0,15(mol)
C+2 -----> C+4 +2e
................0,15...0,3
Cu+2 + 2e ----> Cu
x............2x........x
Fe+3 + 3e ----> Fe
y...........3y........y
theo định luật bảo toàn số mol e, tổng mol e nhường bằng tổng mol e nhận ==>
2x + 3y = 0,3
sau khi td với HNO3
Cu -----> Cu+2+ 2e
x...............x.........2x
Fe-------->Fe+3 + 3e
y..............y............3y
N+5 + 3e -----> N+2
z........3z............z
theo định luật bảo toàn mol e =>2x+3y=3z=0,3
=>z=0,1
=> nNO=0,1 => V=2,24 (l)
#Walker
CO2 + Ba(OH)2 -> BaCO3 + H2O
0,15............................0,15 (mol)
nBaCO3 = 0,15 (mol)
nCO = nCO2 = 0,15 (mol)
Bảo toàn e
N+5 + 3e -> N+2
0,3--> 0,1 (mol)
C+2 + 2e -> C+4
0,15.... ...0,3 (mol)
V = 0,1.22.4=2,24 (l)