Cho m gam Cu tan hoàn toàn vào 200 ml dung dịch HNO3, phản ứng vừa đủ, giải phóng một hỗn hợp 4,48 lít khí NO và NO2 có tỉ khối hơi với H2 là 19. Tính CM của dung dịch HNO3.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


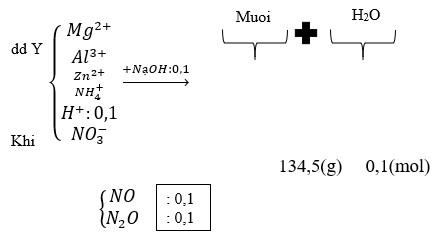
Gọi số mol của Cu là a => nAl= 2a, nMg= 3a
mCu+mAl+mMg = 19 => a=0,1 =>nCu=0,1(mol);nAl=0,2(mol);nMg=0,3(mol)
dY/H2 =18,5 => M(Y)= 37 (dùng pp đường chéo) => nNO=nN2O
n(Y)= \(\dfrac{4,48}{22,4}\) =0,2 (mol)
Suy ra: nNO=nN2O= 0,1 (mol)
nNH4NO3 =\(\dfrac{\text{0,1.2+0,2.3+0,3.2−0,1.3−0,1.8 }}{8}\)=0,0375 (mol) bảo toàn e nhe
mm′ = mCu(NO3)2+ mAl(NO3)3 +mMg(NO3)2+mNH4NO3 = 108,8(g) ( khúc này bảo toàn nguyên tố Cu,Al,Mg => số mol của muối Cu2+,Al3+,Mg2+ )

Đáp án D
Đặt số mol NO là a mol; số mol NO2 là b mol
Suy ra a + b = 0,2 mol; 30a + 46b = 0,2.17.2 = 6,8 gam
Giải hệ trên ta có a = 0,15 và b = 0,05
Quá trình cho e:
Cu → Cu2++ 2e
Quá trình nhận e:
N+5 + 3e → N+2
N+5 + 1e → N+4
Áp dụng định luật bảo toàn e: 2.nCu = 3.nNO + 1.nNO2 → nCu = (3.nNO+ nNO2): 2 = 0,25 mol
Suy ra m = 0,25.64 = 16 gam
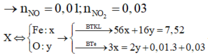
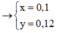
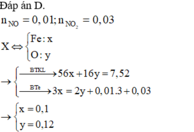
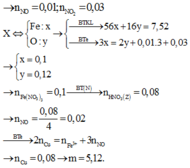
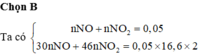
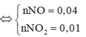


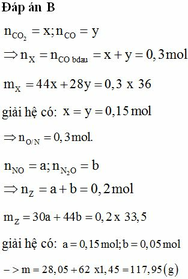
Tham Khảo
nhh = 0.2 mol
Đặt :
nNO = x mol
nNO2 = y mol
<=> x + y = 0.2 mol (1)
\(\overline{M}=\frac{30x+46y}{x+y}=38\)
<=> 30x + 46y = 7.6 (2)
Giải (1) và (2) :
x = y = 0.1
4Cu + 12HNO3 --> 4Cu(NO3)2 + 2NO + 2NO2 + 6H2O
________0.6__________________0.1_____0.1
CM HNO3 = 0.6/0.2=3M