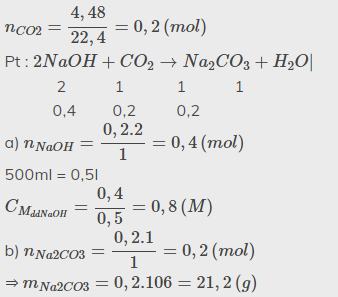Cho 11,2l CO2 vào 500ml dung dịch NaOH 25% (D=1,3g/ml). Tính Cm của dung dịch muối.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{CO_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(m_{ddNaOH}=1,3.500=650\left(g\right)\)
\(\dfrac{m_{ctNaOH}.100\%}{650}=25\%\Rightarrow m_{ctNaOH}=162,5\left(g\right)\)
\(n_{NaOH}=\dfrac{162,5}{40}=4,0625\left(mol\right)\)=>NaOH dư
\(CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\)
0,5-----------------------0,5---------------

Chọn A

=> NaOH dư, C O 2 hết, phản ứng thu được muối N a 2 C O 3
C O 2 + 2 N a O H → N a 2 C O 3 + H 2 O 0 , 5 m o l → 0 , 5 m o l
![]()

a)
C% muối =\(\dfrac{25}{25+35+190}100=10\%\)
C% đường =\(\dfrac{35}{25+35+190}.100=14\%\)
b)
200ml=0,2, x(ml)=0,001x(l)
nNaOH=0,2×3=0,6(mol)
→CMNaOH 1,5M=0,6\0,2+0,001x=1,5M
→x=200

\(n_{CO2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Pt : \(2NaOH+CO_2\rightarrow Na_2CO_3+H_2O|\)
2 1 1 1
0,4 0,2 0,2
a) \(n_{NaOH}=\dfrac{0,2.2}{1}=0,4\left(mol\right)\)
500ml = 0,5l
\(C_{M_{ddNaOH}}=\dfrac{0,4}{0,5}=0,8\left(M\right)\)
b) \(n_{Na2CO3}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{Na2CO3}=0,2.106=21,2\left(g\right)\)
Chúc bạn học tốt

a. PTHH: 2NaOH + CO2 ---> Na2CO3 + H2O
b. Ta có: \(C_{M_{NaOH}}=\dfrac{n_{NaOH}}{500:1000}=0,5M\)
=> nNaOH = 0,25(mol)
Theo PT: \(n_{Na_2CO_3}=\dfrac{1}{2}.n_{NaOH}=\dfrac{1}{2}.0,25=0,125\left(mol\right)\)
Do thể tích dung dịch không đổi sau phản ứng nên:
\(V_{dd_{Na_2CO_3}}=V_{NaOH}=500:1000=0,5\left(lít\right)\)
=> \(C_{M_{Na_2CO_3}}=\dfrac{0,125}{0,5}=0,25M\)

a,\(n_{NaOH}=0,5.1=0,5\left(mol\right);n_{H_2SO_4}=0,5.1=0,5\left(mol\right)\)
PTHH: 2NaOH + H2SO4 → Na2SO4 + 2H2O
Mol: 0,5 0,25 0,25
Ta có: \(\dfrac{0,5}{2}< \dfrac{0,5}{1}\) ⇒ NaOH hết, H2SO4 dư
\(m_{Na_2SO_4}=142.0,25=35,5\left(g\right)\)
b,\(C_{M_{Na_2SO_4}}=\dfrac{0,25}{1}=0,25M\)
\(C_{M_{H_2SO_4dư}}=\dfrac{0,5-0,25}{1}=0,25M\)