Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
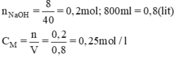
b) nNaOH có trong 200ml dung dịch NaOH 0,25M là

VH2O cần dùng để pha loãng 200ml dung dịch NaOH 0,25M để dung dịch NaOH 0,1M.
VH2O = 500 - 200 = 300ml H2O.

a) mNaOH trong dd 10%=mNaOH ban đầu=40.10%=4gam
mH2O trong dd ban đầu=40-4=36gam
b) khi thêm H2O lượng NaOH không đổi=4 gam
=>mdd NaOH4%=4/4%=100gam
Gọi mH2O thêm=x gam
mdd sau pứ=x+40 gam
=>x=100-40=60 gam
Vậy cần thêm 60 gam H2O
E ngj thế nay hợp lí hơn ak:
mNaOH có trong 40g đ NaOH 10% là: 40.10%
mđNaOH 4% là: 4;4%= 100g
mH2O thêm vào là: 100-40=60g

Ukm... E mới lp6 nên k bjết đux ko nha:
mNaOH có trong 40g đ NaOH 10% là: 40.10%=4g
mddNaOH 4% là 4 : 4%= 100g
mH2O (là nc ak) thêm vào là: 100-40=60g
Ah, a xem trog "Bồi dg năg lực tự học Hoá học 8" pải k ak, nó có sẵn đáp số nên e lm cả cách lm rồi ak. A cứ kjểm tra laj xem ak...

\(n_{NaOH}\left(dd1\right)=\dfrac{20}{40}=0,5\left(mol\right)\)
\(n_{NaOH}\left(dd2\right)=0,25.1,5=0,375\left(mol\right)\)
\(Vddsau=0,8+1,5=2,3(l)\)
\(n_{NaOH}\left(sau\right)=0,5+0,375=0,875\left(mol\right)\)
CM của dung dịch sau khi trộn .
\(C_{M_{NaOH}}\left(sau\right)=\dfrac{0,875}{2,3}\approx0,38\left(M\right)\)

mNaOH = 200.10% = 20 gam ➝ nNaOH = 0,5 mol
nH2SO4 = 0,1 mol, nMgSO4 = 0,2 mol
Phản ứng:
(1) 2NaOH + H2SO4 ➝ Na2SO4 + 2H2O
0,2 0,1 0,1 (mol)
(2) 2NaOH + MgSO4 ➝ Mg(OH)2 + Na2SO4
0,3 0,15 0,15 0,15 (mol)
Dung dịch X: Na2SO4: 0,25 mol, MgSO4 dư: 0,05 mol
Kết tủa Mg(OH)2: 0,15 mol
Mg(OH)2 ➝ MgO + H2O
0,15 0,15
m1 = 0,15.58 = 8,7 gam
m2 = 0,15.40 = 6 gam
nNaOH=\(\dfrac{48}{40}\)=1,2(mol)
=>Cm ban đầu =\(\dfrac{1,2}{x}\)
Cm mới=\(\dfrac{1,2}{x+0,5}\)M
=> \(\dfrac{\dfrac{1,2}{x}}{\dfrac{1,2}{0,5+x}}=2\)
<=> x=0,5
=>Cm bđ =\(\dfrac{1,2}{0,5}=2,4M\)