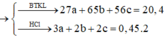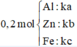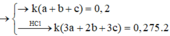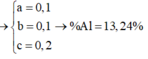Cho hỗn hợp Al và Zn có số mol bằng nhau tác dụng vừa đủ với dung dịch HCl thu được 6,72 lít
khí H2. Khối lượng Al và Zn trong hỗn hợp lần lượt là:
Giúp mk vs ạ, thanks nhiều nhé!!!!
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Gọi nAl = nZn = a (mol)
\(n_{H_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
a---------------------->1,5a
Zn + 2HCl --> ZnCl2 + H2
a--------------------->a
=> 1,5a + a = 0,6
=> a = 0,24 (mol)
=> mhh = 0,24.27 + 0,24.65 = 22,08 (g)
Gọi \(n_{Al}=n_{Zn}=a\left(mol\right)\)
PTHH:
2Al + 6HCl ---> 2AlCl3 + 3H2
a a
Zn + 2HCl ---> ZnCl2 + H2
a a
\(\rightarrow22,4\left(a+a\right)=13,44\\ \Leftrightarrow a=0,3\left(mol\right)\\ \rightarrow\left\{{}\begin{matrix}m_{Al}=0,3.27=8,1\left(g\right)\\m_{Zn}=0,3.65=19,5\left(g\right)\end{matrix}\right.\\ \rightarrow m_{hh}=8,1+19,5=27,6\left(g\right)\)

Đáp án D
Xét trường hợp 20,4 gam A tác dụng với dung dịch HCl dư:
Gọi số mol các chất là Al: a mol; Zn: b mol; Fe: c mol
Ta có:

Các quá trình nhường, nhận electron:
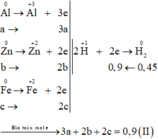
Xét trường hợp 0,2 mol A tác dụng với Cl2:
Gọi số mol các chất là Al: ka mol; Zn: kb mol; Fe: kc mol
Ta có:
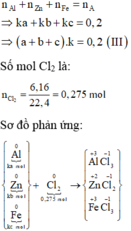
Các quá trình nhường, nhận electron:
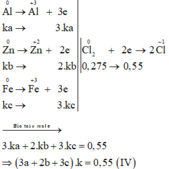
Lấy (IV) chia (III) vế với vế ta được:


Đáp án : D
Gọi số mol Al ; Zn ; Fe lần lượt là x ; y ; z
=> 27x + 65y + 56z = 20,4 (1)
Và 1,5x + y + z = nH2 = 0,45 (2)
Xét 0,2 mol X có lượng chất gấp t lần 20,4g X
=> t(x + y +z) = 0,2 mol (3)
Lại có : Bảo toàn e : 2nCl2 = (3x + 2y + 3z)t = 0,55 (4)
Từ (1),(2),(3),(4) => x = y = 0,1 ; z = 0,2
=> %mAl(X) = 13,24%

ta có n Mg=nZn
=>n H2=0,2 mol
->n Zn=n Mg=0,1 mol
=>m Mg=0,1.24=2,4g
=>B

TN1: Gọi (nAl; nZn; nFe) = (a; b; c)
=>27a + 65b + 56c = 20,4 (1)
\(n_{H_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
a----------------------->1,5a
Zn + 2HCl --> ZnCl2 + H2
b--------------------->b
Fe + 2HCl --> FeCl2 + H2
c----------------------->c
=> \(1,5a+b+c=0,45\) (2)
TN2: Gọi (nAl; nZn; nFe) = (ak; bk; ck)
=> ak + bk + ck = 0,2 (3)
\(n_{Cl_2}=\dfrac{6,16}{22,4}=0,275\left(mol\right)\)
PTHH: 2Al + 3Cl2 --to--> 2AlCl3
ak-->1,5ak
Zn + Cl2 -to-> ZnCl2
bk--->bk
2Fe + 3Cl2 --to--> 2FeCl3
ck--->1,5ck
=> 1,5ak + bk + 1,5ck = 0,275 (4)
(1)(2)(3)(4) => \(\left\{{}\begin{matrix}a=0,1\left(mol\right)\\b=0,1\left(mol\right)\\c=0,2\left(mol\right)\end{matrix}\right.\)
=> \(\%Fe=\dfrac{0,2.56}{20,4}.100\%=54,9\%\)