Bài 6: Nhiệt phân 6,86g đồng (II) hidroxit đến khi phản ứng hoàn toàn thu được m gam chất rắn. a. Tính giá trị m b. Cho toàn bộ chất rắn trên tác dụng với hoàn toàn với dung dịch HC1 15% thì thu được dung dịch X. Tính C% của dung dịch X
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
4Na2Cr2O7 → t 0 4Na2CrO4 + 2Cr2O3 + 3O2
Có

A + Ba(OH)2 → BaCrO 4 : 0 , 08 + 2 . 0 , 02 = 0 , 12 mol Cr 2 O 3 : 0 , 04 mol
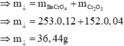

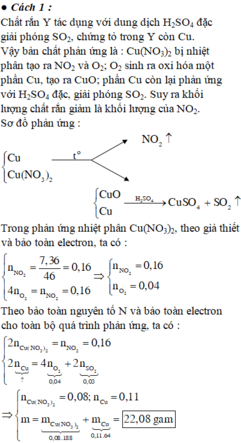
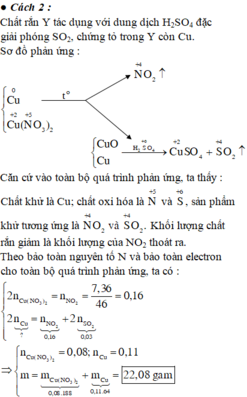
Do Y tác dụng với H 2 S O 4 tạo S O 2 nên Y có Cu.
Do đó khối lượng chất rắn giảm là khối lượng của N O 2

Đáp án là D

Chọn đáp án B
Trong 50 gam dung dịch NaOH chứa 36 gam nước ( 2 mol) và 14 gam NaOH (0,35 mol)
Chất lỏng Z gồm ancol đơn chức x mol và nước 2 mol
Cho Z tác dụng với Na dư
→ n H 2 = 1 , 1 = 0 , 5 . 2 + 0 , 5 . x
→ x = 0,2 mol
Có mancol = 42,4- 36 = 6,4 gam
→ Mancol = 32 (CH3OH)
Vì este đơn chức nên
nA = nancol = 0,2 mol
→ MA = 86 (C4H6O2)
Vậy A có công thức CH2=CH-COOCH3
Chất rắn thu được gồm
CH2=CH-COONa: 0,2 mol,
NaOH dư : 0,35- 0,2 = 0,15 mol
C H 2 = C H - C O O N a + N a O H → t 0 , C a O C H 2 = C H 2 + N a 2 C O 3


mZ = 2.18 + 0,2.M ancol = 42,4 => M ancol = 32 => Ancol là CH3OH
n este = n ancol = n muối = nNaOH pư = 0,2 mol => M este = 17,2 : 0,2 = 86
=> CTCT este: CH2=CH-COOCH3 => Y gồm CH2=CH-COONa (0,2 mol) và NaOH dư (0,15 mol)
CH2=CH-COONa + NaOH 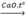 CH2=CH2 + Na2CO3
CH2=CH2 + Na2CO3
Bđ: 0,2 0,15
Pư: 0,15 ← 0,15 → 0,15
=> m = 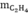 = 0,15.28 = 4,2 gam
= 0,15.28 = 4,2 gam
Đáp án cần chọn là: D

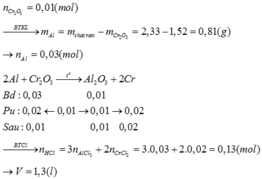

a, \(n_{Cu\left(OH\right)_2}=\dfrac{6,86}{98}=0,07\left(mol\right)\)
PTHH: Cu(OH)2 ---to→ CuO + H2O
Mol: 0,07 0,07
\(m_{CuO}=0,07.80=5,6\left(g\right)\)
b,
PTHH: CuO + 2HCl → CuCl2 + H2O
Mol: 0,07 0,14 0,07
\(m_{ddHCl}=\dfrac{0,14.36,5.100}{15}=\dfrac{511}{15}\left(g\right)\)
mdd sau pứ = \(5,6+\dfrac{511}{15}=\dfrac{119}{3}\left(g\right)\)
\(C\%_{ddCuCl_2}=\dfrac{0,07.135.100\%}{\dfrac{119}{3}}=23,82\%\)