Hỗn hợp X gồm CH4, C2H2, C2H4. Đốt cháy 15g hỗn hợp X thu được 48,4g CO2. Nếu lấy 16,128l khí X vừa đủ làm mất màu dung dịch chứa 153,6g Br2. Tìm thành phần phần trăm khối lượng các khí trong X
giúp em với em cần gấp!!!
em cảm ơn ạ!!!
@Cẩm Vân Nguyễn Thị @Trương Hồng Hạnh@Hoàng Nhất Thiên@Phùng Hà Châu@Hoàng Thảo Linh@Trần Hữu Tuyển


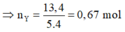
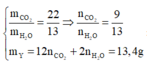
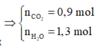
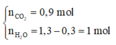
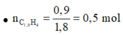
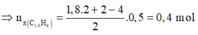
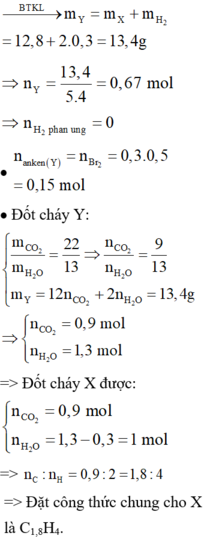
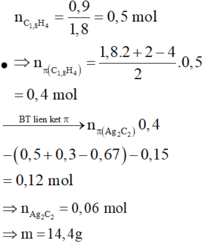
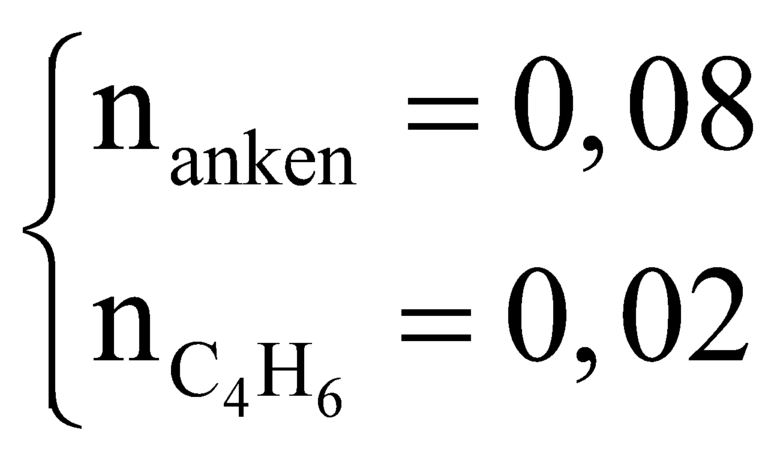

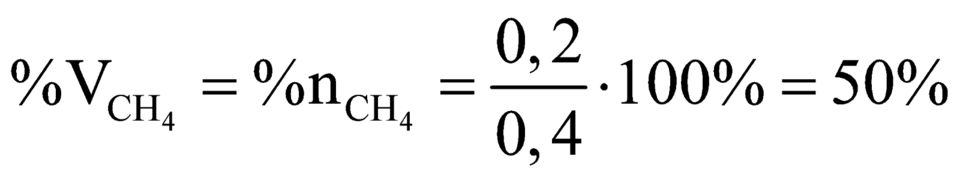
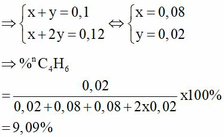

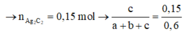
X gồm: CH4, C2H2, C2H4
Các phương trình đốt cháy:
CH4 + 2O2 => CO2 + 2H2O
C2H4 + 3O2 => 2CO2 + 2H2O
C2H2 + 5/2 O2 => 2CO2 + H2O
Các phương trình tác dụng Br2: (CH4 không t/d Br2)
C2H4 + Br2 => C2H4Br2
C2H2 + 2Br2 => C2H2Br4
nCO2 = m/M = 48.4/44 = 1.1 (mol)
nBr2 = m/M = 153.6/160 = 0.96 (mol)
nX = V/22.4 = 16.128/22.4 = 0.72 (mol)
Gọi x,y,z (mol) lần lượt là số mol của CH4, C2H4 và C2H2
Ta có: 16x + 28y + 26z = 15 (g) (1)
x + 2y + 2z = nCO2 = 1.1 (mol) (2)
a( x + y + z ) = 0.72 (mol)
a(y + 2z) = 0.96 (mol)
Suy ra: \(\frac{x+y+z}{y+z+z}=\frac{0.72}{0.96}\)
0.96x + 0.96y + 0.96z = 0.72y + 1.44z
==> 0.96x + 0.24y - 0.48z = 0 (3)
Từ (1), (2), (3)
Dùng máy tính để giải, ta được:
x = 0.1 (mol), y = 0.2 (mol), z = 0.3 (mol)
mCH4 = n.M = 16x = 16 x 0.1 = 1.6 (g)
mC2H4 = n.M = 28y = 28 x 0.2 = 5.6 (g)
mC2H2 = n.M = 26z = 26 x 0.3 = 7.8 (g)
mhh = 15 (g) (theo đề bài)
Tính % khối lượng các khí trong hỗn hợp X
C%mCH4 = 1.6 x 100/15 = 10.67 (%)
C%mC2H4 = 5.6 x 100/15 = 37.33 (%)
C%mC2H2 = 7.8 x 100/15 = 52 (%)