Cho 11,9g hỗn hợp Al và Zn tác dụng hết với dd H2SO4 đặc nóng thu được 8.96 l khí SO2 ở đktc.
a) viết pt phản ứng và tính % về khối lượng của Al và Zn trong hỗn hơp ban đầu
b) hấp thụ lượng SO2 vào 500ml đ NAOH 2M. Tính khối lượng các chất thu được sau phảm ứng.
Mọi người chỉ giúp em câu b) với ạ

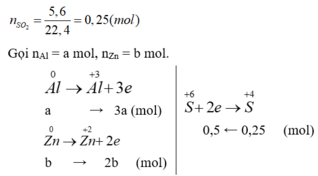



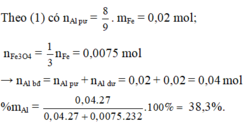



Đặt: nAl= x (mol)
nZn= y (mol)
mhh= 27x + 65y= 11.9g (1)
2Al + 6H2SO4(đ) -to-> Al2(SO4)3 + 3SO2 + 6H2O
Zn + 2H2SO4(đ) -to-> ZnSO4 + SO2 + 2H2O
nH2= 1.5x + y=8.96/22.4=0.4 (mol) (2)
Giải pt (1) và (2):
x=0.2
y=0.1
mAl= 5.4g
mZn= 6.5g
%Al= 45.37%
%Zn= 54.63%
nNaOH= 0.5*2=1 (mol)
T= 1/0.4=2.5 => tạo ra muối NaHSO3
NaOH + SO2 --> NaHSO3
nNaHSO3= 0.4 (mol)
mNaHSO3= 41.6g
Câu b:
nSO2 = V/22.4 = 8.96/22.4 = 0.4 (mol)
nNaOH = CM.V = 0.5 x 2 = 1 (mol)
nNaOH / nSO2 = 1/0.4 = 2.5 >2
=> chỉ thu muối trung hòa
2NaOH + SO2 => Na2SO3 + H2O
mNa2SO3 = n.M = 0.4 x 126 = 50.4 (g)
mNaOH dư = n.M = 0.2 x 40 = 8 (g)