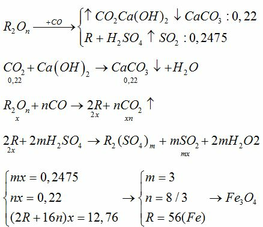Hòa tan 10,2g RxOy vào dung dịch H2SO4 có chứa0,3 mol H2SO4. Tìm CTHH của RxOy
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi oxit kim loại cần tìm là R2On (n là hóa trị của kim loại cần tìm)
R2On +3H2SO4 -----------> R2(SO4)n +3H2O
m dung dịch sau pứ= 10,2 + 331,8 = 342 (g)
C%dd muối = \(\dfrac{m_{R_2\left(SO_{\text{4}}\right)_n}}{342}.100=10\)
=>m R2(SO4)n =34,2 (g)
Ta có : \(n_{R_2O_n}=n_{R_2\left(SO_4\right)_n}\)
=> \(\dfrac{10,2}{2R+16n}=\dfrac{34,2}{2R+96n}\)
Lập bảng :
| n | 1 | 2 | 3 |
| R | 9 | 18 | 27 |
| Kết luận | Loại | Loại | Chọn (Al) |
Vậy CTHH của oxit kim loại là Al2O3

PTHH :
RxOy + 2yHCl \(\rightarrow\) xRCl2y/x + yH2O.
Theo PTHH : nRxOy = \(\dfrac{1}{2y}\) nHCl =\(\dfrac{0.3}{2y}\)(mol)
\(\Rightarrow\) MRxOy = \(\dfrac{12}{\dfrac{0.3}{^{ }2y}}\)= 80y
\(\Leftrightarrow\)Rx + 16y = 80y
\(\Leftrightarrow\)Rx=64y
\(\Leftrightarrow\)R=\(\dfrac{64y}{x}\)
\(\Leftrightarrow\)R = 32\(\dfrac{2y}{x}\)
Vì \(\dfrac{2y}{x}\)là hóa trị của R nên ta có :
| \(\dfrac{2y}{x}\) | 1 | 2 | 3 |
| R | 32 | 64 | 96 |
| Loại | Cu | Loại |
Vậy CT oxit cần tìm là CuO
\(R_xO_y+2yHCl\rightarrow xRCl_{\dfrac{2y}{x}}+yH_2O\)
\(\dfrac{0,3}{2y}\)<-------0,3
\(\Rightarrow M_{R_xO_y}=\dfrac{m}{n}=\dfrac{12}{\dfrac{0,3}{2y}}=80y\Leftrightarrow M_R.x+16y=10y\)
\(\Leftrightarrow M_R=64\dfrac{x}{y}\)
Cặp x; y thõa mãn là x = 2; y = 2==> MR =64
Vậy công thức oxit là CuO

Đấp án B
RxOy, khi tan trong nước tạo ra hai axit kém bền (chỉ tồn tại trong dung dịch), khi tan trong kiềm tạo ion RO42- có màu vàng → Oxit là CrO3.
- CrO3 có tính oxi hóa mạnh
- CrO3 + H2O → H2CrO4
2CrO3 + H2O → H2Cr2O7
Hai axit H2CrO4, H2Cr2O7 không tách ra ở dạng tự do, chỉ tồn tại trong dung dịch. Nếu tách khỏi dung dịch, chúng sẽ bị phân hủy trở lại CrO3.![]()

\(C_{M\left(dd.H_2SO_4.sau.khi.trộn\right)}=\dfrac{0,5.0,5+0,3.1,5}{0,5+0,3}=0,875M\)

\(Coi\ m_{dd\ H_2SO_4} = 98(gam)\\ n_{H_2SO_4}= \dfrac{98.10\%}{98} = 0,1(mol)\\ R_2O_n + nH_2SO_4 \to R_2(SO_4)_n + nH_2O\\ n_{R_2O_n} = n_{R_2(SO_4)_n} = \dfrac{1}{n}n_{H_2SO_4} = \dfrac{0,1}{n}(mol)\\ m_{dd\ sau\ pư} = m_{oxit} + m_{dd\ H_2SO_4} = \dfrac{0,2R}{n} + 99,6(gam)\\ C\%_{muối} = \dfrac{\dfrac{0,1}{n}(2R + 96n)}{\dfrac{0,2R}{n} +99,6}.100\% = 12,9\%\\ \Rightarrow \dfrac{R}{n }=18,64\)
Với n = 3 thì R = 56(Fe)
Vậy oxit là Fe2O3
Cho hỏi tại sao khi chưa có căn cứ gì người giải lại tự coi m dd H2SO4 =98g ạ

a) \(n_{H_2}=\dfrac{0,8}{2}=0,4\left(mol\right)\)
PTHH: 2A + H2SO4 --> A2SO4 + H2
0,8<-------------------------0,4
=> \(M_A=\dfrac{18,4}{0,8}=23\left(Na\right)\)
b)
PTHH: 2Na + H2SO4 --> Na2SO4 + H2
0,4<--------0,4<----0,4
=> \(C_{M\left(ddH_2SO_4\right)}=\dfrac{0,4}{0,5}=0,8M\)
\(C_{M\left(ddNa_2SO_4\right)}=\dfrac{0,4}{0,5}=0,8M\)