tại sao ở điều kiện thường, H2O tồn tại ở thể lỏng còn các hidrua khác trong nhóm lại ở thể khí?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


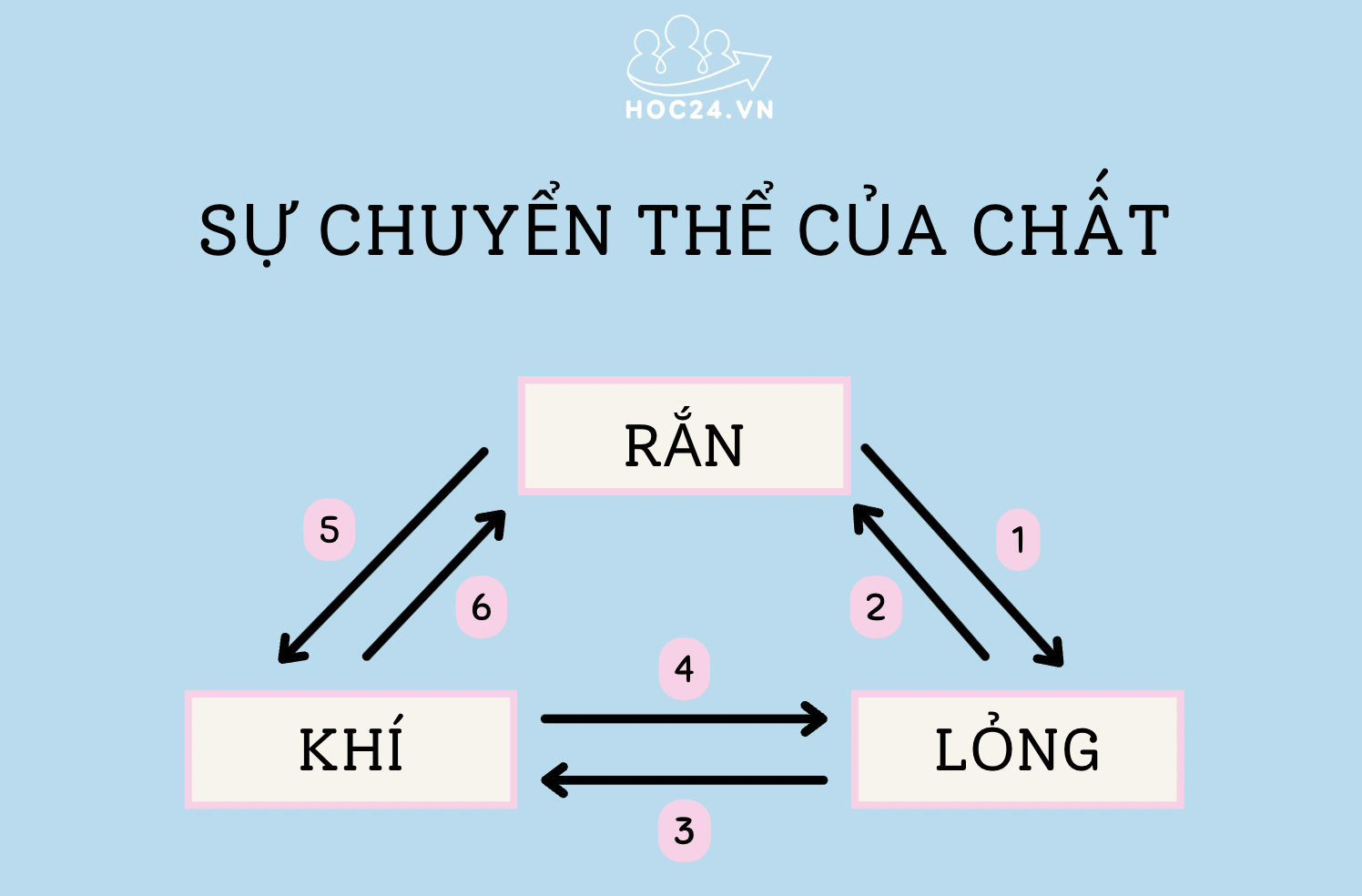
1. Thể rắn sang thể lỏng: sự nóng chảy.
2.Thể lỏng sang thể rắn:sự đông đặc
3.Thể lỏng sang thể khí:sự hóa hơi
4.Thể khí sang thể lỏng:sự ngưng tụ
5.Thể rắn sang thể khí:sự thăng hoa
6.Thể khí sang thể rắn:sự ngưng kết
(1): Sự nóng chảy
(2): Sự đông đặc
(3): Sự bay hơi
(4): Sự ngưng tụ
(5): Sự thăng hoa
(6): Sự ngưng tụ

Khi ở nhiệt độ cao và áp suất khác, nước sẽ phân hủy thành O2 với H2
tham khảo
Khi ở nhiệt độ cao và áp suất khác, nước sẽ phân hủy thành o2 với H2

Chọn đáp án B
Ở điều kiện thường, fructozơ, saccarozơ và glucozơ đều là chất rắn kết tinh; triolein là chất lỏng

H2O có liên kết Hidro còn H2S thì không có. Liên kết Hidro làm cho các phân tử nước liên kết lại với nhau, nhờ đó, nước ở thể lỏng còn H2S ở thể khí. Còn vì sao có liên kết Hidro thì không nhớ rõ nữa, hình như Oxy có độ âm điện lớn hơn Hidro, hút electron của Hidro về phía mình, do đó, nguyên tử O sẽ tích điện âm, H thiếu e nên tích điện dương. Nhờ vậy, nguyên tử H này lại liên kết với nguyên tử O của phân tử nước khác tạo thành liên kết Hidro.

Đặc điểm hợp chất ion:
+ Các hợp chất ion thường là tinh thể rắn ở điều kiện thường
+ Hợp chất ion có nhiệt độ nóng chảy và nhiệt độ sôi rất cao
=> Phát biểu (b) và (c) đúng

Chọn A.
A. O2 và Cl2: không phản ứng dù là nhiệt độ cao;
B. NH3 và Cl2: 2NH3 + 3Cl2 → S + 2HCl;
C. H2S và Cl2: H2S + Cl2
→
S + 2HCl;
D. HI và Cl2: 2HI + Cl2
→
I2 + 2HCl

H2O ở thể lỏng, trong khi các hợp chất của hiđro khác như BH3, CH4, NH3, H2S, ... đều ở thể khí, vì các phân tử nước hút nhau bằng liên kết hiđro rất mạnh, làm cho các phân tử nước liên kết chặt chẽ. (Còn ở BH3, CH4 chúng không có liên kết hiđro, nên các phân tử không thể liên kết được với nhau).