1)1 hỗn hợp A gồm 1 oxit và muối cacbonat của kim loại M có hóa trị II có khối lượng 20,4 gam tác dụng vừa đủ với 0,8mol HCl sau phản ứng thu được V lít CO2.kim loại M và ía trị của V là?
help me với .thank nhìu
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Đặt số mol của MO, M(OH)2, MCO3 tương ứng là x, y, z.
Nếu tạo muối trung hòa ta có các phản ứng:
MO + H2SO4 →MSO4 + H2O (1)
M(OH)2 + H2SO4 →MSO4 + 2H2O (2)
MCO3 + H2SO4 →MSO4 + H2O + CO2 (3)
Nếu tạo muối axít ta có các phản ứng:
MO + 2H2SO4 →M(HSO4)2 + H2O (4)
M(OH)2 + 2H2SO4 →M(HSO4)2 + 2H2O (5)
MCO3 + 2H2SO4 →M(HSO4)2 + H2O + CO2 (6)
Ta có :
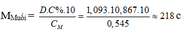
– TH1: Nếu muối là MSO4 M + 96 = 218 M = 122 (loại)
– TH2: Nếu là muối M(HSO4)2 M + 97.2 = 218 M = 24 (Mg)
Vậy xảy ra phản ứng (4, 5, 6) tạo muối Mg(HSO4)2
b) Theo (4, 5, 6) Số mol CO2 = 0,448/22,4 = 0,02 molz = 0,02 (I)
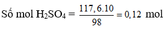
2x + 2y + 2z = 0,12 (II)
Đề bài: 40x + 58y + 84z = 3,64 (III)
Giải hệ (I, II, III): x = 0,02; y = 0,02; z = 0,02
%MgO = 40.0,02.100/3,64 = 21,98%
%Mg(OH)2 = 58.0,02.100/3,64 = 31,87%
%MgCO3 = 84.0,02.100/3,64 = 46,15%

Đáp án D
Có

m g X + HNO3 đặc nguội → 0,1 mol NO2
→ BTe a . n M = 0 , 1 m o l ( 2 )
Từ (1) và (2) suy ra:
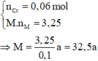
=> a = 2, M = 65 (M là Zn).

Đáp án D
Đặt công thức của hai muối là RCO3: x mol
RCO3+ 2HCl → RCl2+ CO2+ H2O
x 2x x x mol
Theo định luật bảo toàn khối lượng:
mmuối cacbonat+ mHCl= m muối clorua+ mCO2+ mH2O
→ 7,0 + 2x. 36,5=9,2+ 44x+18x → x= 0,2 mol→ VCO2= 0,2.22,4= 4,48 lít

Đáp án C
Gọi công thức của hai muối trong hỗn hợp ban đầu là A2CO3 và BCO3.
Có các phản ứng:
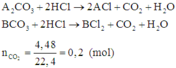
Quan sát phản ứng thấy khi cho hỗn hợp phản ứng với dung dịch HCl thì mỗi gốc C O 3 2 - trong muối được thay thế bởi hai gốc Cl-.
Có 1 mol C O 3 2 - bị thay thế bởi 2 mol Cl- thì khối lượng của muối tăng: (2.35,5 -60) = 11(gam)
Do đó khối lượng muối khan thu được khi cô cạn dung dịch là:
mmuối clorua = mmuối cacbonat + 0,2.11 = 23,8 + 0,2.11= 26 (gam)

Bài 1:
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\\ n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2\\ n_{Al}=\dfrac{2}{3}.0,3=0,2\left(mol\right)\\ \Rightarrow m_{Al}=0,2.27=5,4\left(g\right)\\ \%m_{Al}=\dfrac{5,4}{26,82}.100\approx20,134\%\\\Rightarrow \%m_{Al_2O_3}\approx79,866\%\\ b,n_{Al_2O_3}=\dfrac{26,82-5,4}{102}=0,21\left(mol\right)\\ n_{HCl}=6.0,21+2.0,3=1,86\left(mol\right)\\ V_{ddHCl}=\dfrac{1,86}{2}=0,93\left(l\right)=930\left(ml\right)\\ m_{ddHCl}=930.1,12=1041,6\left(g\right)\\ n_{AlCl_3}=2.0,21+0,2=0,62\left(mol\right)\\ C\%_{ddAlCl_3}=\dfrac{0,62.133,5}{1041,6-0,3.2}.100\approx7,951\%\)
2)
a) Gọi KL và oxit của nó là M và MO
nHCl = 4.0,25 = 1 (mol)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: M + 2HCl --> MCl2 + H2
0,3<-0,6<--------------0,3
MO + 2HCl --> MCl2 + H2O
0,2<---0,4
=> 0,3.MM + 0,2.(MM + 16) = 31,2
=> MM = 56 (g/mol)
=> Kim loại là Sắt (Fe)
b)
\(\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{0,3.56}{31,2}.100\%=53,85\%\\\%m_{FeO}=\dfrac{0,2.72}{31,2}.100\%=46,15\%\end{matrix}\right.\)
MO+2HCl\(\rightarrow\)MCl2+H2O
x 2x (mol)
MCO3+2HCl\(\rightarrow\)MCl+CO2+H2O
y 2y (mol)
\(\overline{M}\)của MO và MCO3 là \(\dfrac{M+16+M+12+16.3}{2}\)=M+38
mà \(\overline{M}\)=\(\dfrac{20.4}{x+y}\)=\(\dfrac{20,4}{0,2}\) =102(vì 2x+2y=0,4)0.8 là sai đề
\(\Rightarrow\)M=64\(\Rightarrow\)M là Cu
\(\left\{{}\begin{matrix}x+y=0,2\\80x+124y=20,4\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
\(\Rightarrow\)VCO2=0,1.22,4=2,24
x là mol của MO,2x là mol của HCl
y là mol của MCO3 ,2y là mol của HCl