Tính nồng độ mol/lit của các ion sau a, 100ml dung dịch chứa 4.26 gam al(no3)3 b, 400ml dung dịch Fe2(SO4)3 0,2M
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

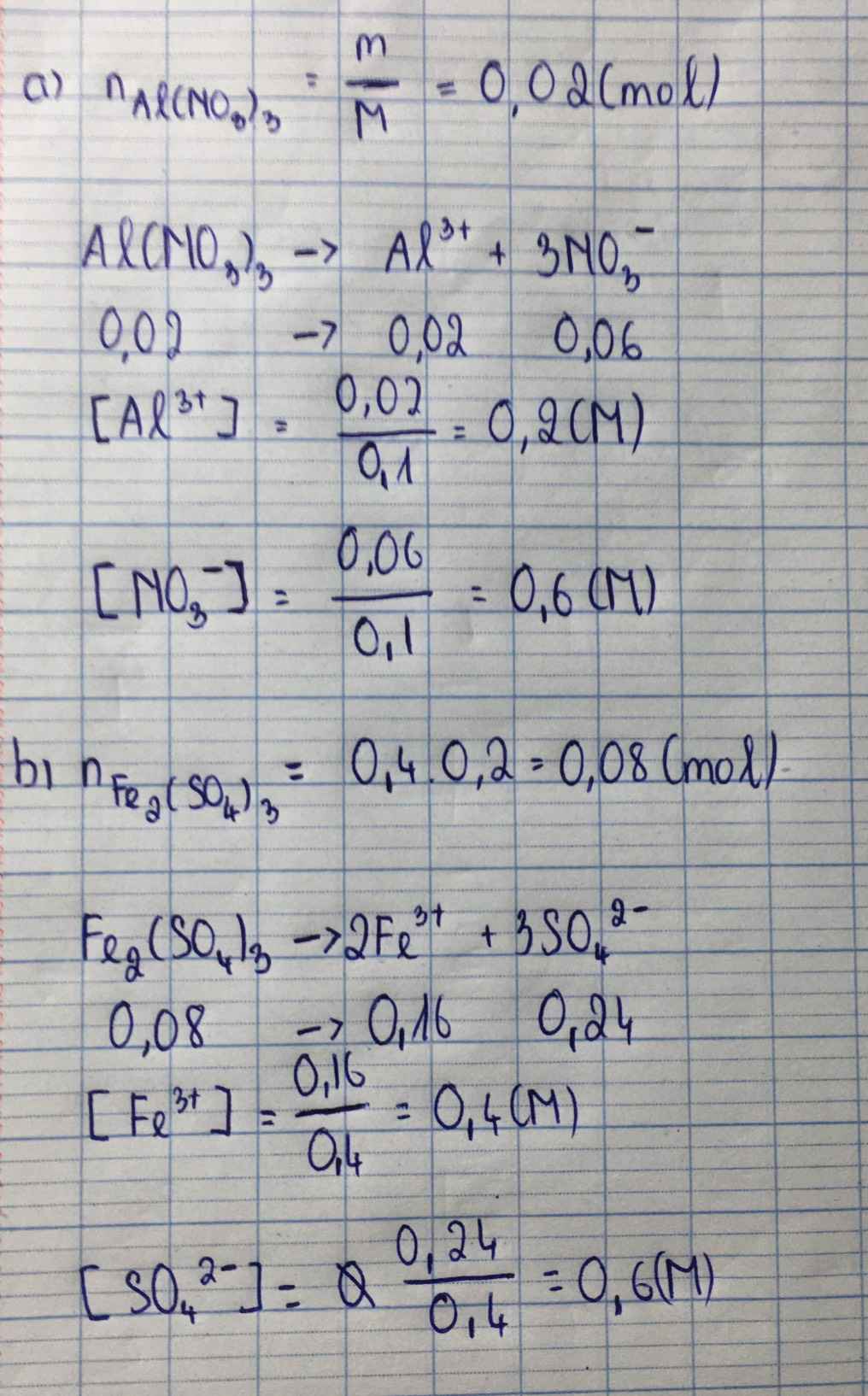

a) Ta có: \(n_{Al\left(NO_3\right)_3}=\dfrac{4,26}{213}=0,02\left(mol\right)\) \(\Rightarrow\left\{{}\begin{matrix}n_{Al^+}=0,02\left(mol\right)\\n_{NO_3^-}=0,06\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\left[Al^+\right]=\dfrac{0,02}{0,1}=0,2\left(M\right)\\\left[NO_3^-\right]=\dfrac{0,06}{0,1}=0,6\left(M\right)\end{matrix}\right.\)
b) Ta có: \(\left[Na^+\right]=0,1+0,02\cdot2+0,3=0,304\left(M\right)\)
c) Bạn xem lại đề !!

PTHH: \(Fe_2\left(SO_4\right)_3+6NaOH\rightarrow3Na_2SO_4+2Fe\left(OH\right)_3\downarrow\)
\(Al_2\left(SO_4\right)_3+6NaOH\rightarrow3Na_2SO_4+2Al\left(OH\right)_3\downarrow\)
Ta có: \(n_{NaOH\left(p/ứ\right)}=6n_{Fe_2\left(SO_4\right)_3}+6n_{Al_2\left(SO_4\right)_3}=6\cdot\left(\dfrac{8}{400}+\dfrac{13,68}{342}\right)=0,36\left(mol\right)\)
Mà \(\Sigma n_{NaOH}=\dfrac{16,8}{40}=0,42\left(mol\right)\) \(\Rightarrow n_{NaOH\left(dư\right)}=0,06\left(mol\right)\)
PTHH: \(NaOH+Al\left(OH\right)_3\rightarrow NaAlO_2+2H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{Al\left(OH\right)_3}=2n_{Al_2\left(SO_4\right)_3}=0,08\left(mol\right)\\n_{NaOH\left(dư\right)}=0,06\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) NaOH p/ứ hết
\(\Rightarrow\left\{{}\begin{matrix}n_{Na_2SO_4}=0,04\cdot3+0,02\cdot3=0,18\left(mol\right)\\n_{NaAlO_2}=0,06\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}C_{M_{Na_2SO_4}}=\dfrac{0,18}{0,5}=0,36\left(M\right)\\C_{M_{NaAlO_2}}=\dfrac{0,06}{0,5}=0,12\left(M\right)\end{matrix}\right.\)

2)
nKOH = 0.15*2=0.3 mol
nHCl = 0.25*3=0.75 mol
KOH + HCl --> KCl + H2O
Bđ: 0.3____0.45
Pư : 0.3____0.3____0.3
Kt: 0______0.15___0.3
DD sau phản ứng : 0.15 mol HCl dư , 0.3 mol KCl
CM H+= 0.15/0.25=0.6M
CM Cl- = 0.15/0.25=0.6 M
CM K+= 0.3/(0.15+0.25)=0.75M
CM Cl-= 0.3/(0.15+0.25)= 0.75M

Đáp án D
• 0,42 mol NaOH + 0,02 mol Fe2(SO4)3; 0,04 mol Al2(SO4)3 → 500ml X + ↓
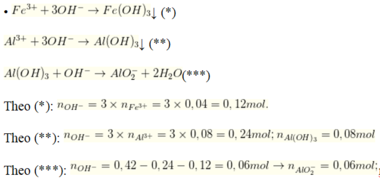
nAl(OH)3 = 0,08 - 0,06 = 0,02 mol
Vậy sau phản ứng 500ml dung dịch X gồm 0,06 mol Na[Al(OH)4]; 0,18 mol Na2SO4
→ CM các chất trong X là CMNa2SO4 = 0,06 : 0,5 = 0,12 M;
CMNa[Al(OH)4] = 0,18 : 0,5 = 0,36 M

a, \(\left[Al^{3+}\right]=0,2.2=0,4\left(M\right)\)
\(\left[SO_4^{2-}\right]=0,2.3=0,6\left(M\right)\)
b, \(\left[Mg^{2+}\right]=0,15.1=0,15\left(M\right)\)
\(\left[Cl^-\right]0,15.2=0,3\left(M\right)\)

