Tính khối lượng của mối thu được trong các trường hợp sau
a) hòa tan 2,24 lít CO2(đktc) vào 100g dd Ca(OH) 7,4%
b) hòa tan 2,24 lít CO2(đktc) vào 100g dd Ca(OH) 3,7 %
c) hòa tan 2,24 lít CO2 (ĐKTC) vào 100g dd Ca(OH) 5%
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nCO2 = \(\dfrac{2,24}{22,4}\) = 0,1 (mol)
nCaCO3 = 0,1 (mol)
PT: CO2(k) + Ca(OH)2(dd) -----> CaCO3(r) + H2O(l)
Theo pt ta có: nCaCO3 = nCa(OH)2 ( hoặc = nCO2 ) = 0,1 (mol)
=> mCaCO3 = 0,1 . 100 = 10 (g)
Các ý dưới tương tự. Nhưng ông nhớ xét dư nha vì ý a hết nên tôi không ghi

Đáp án B
Gọi a, b lần lượt là số mol của Fe, Cu
56a + 64b = 14,8 (1)
Quá trình nhường electron:
Fe - 3e → Fe
a 3a
Cu - 2e → Cu
b 2b
→ ∑ne nhường = (3a + 2b) mol
Quá trình nhận electron:
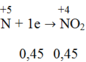
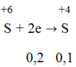
→ ∑ne nhận = 0,45 + 0,2 = 0,65 mol
Áp dụng định luật bảo toàn electron:
3a + 2b = 0,65 → a = 0,15 và b = 0,1 → mFe = 8,4 g

Giải:
Số mol của H2 là:
nH2 = V/22,4 = 19,6/22,4 = 0,875 (mol)
Gọi nMg = x (mol) và nAl = y (mol)
PTHH: Mg + 2HCl -> MgCl2 + H2↑
---------x--------------------------x--
PTHH: 2Al + 6HCl -> 2AlCl3 + 3H2↑
----------y-----------------------------\(\dfrac{3}{2}y\)--
Ta có hệ phương trình:
\(\left\{{}\begin{matrix}m_{Mg}=m_{Al}\\n_{H_2}=0,875\left(mol\right)\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}24x-27y=0\\x+\dfrac{3}{2}y=0,875\left(mol\right)\end{matrix}\right.\)
Giải hệ phương trình, ta được:
\(\left\{{}\begin{matrix}x=0,375\left(mol\right)\\y=\dfrac{1}{3}\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Mg}=n.M=0,375.24=9\left(g\right)\\m_{Al}=n.M=\dfrac{1}{3}.27=9\left(g\right)\end{matrix}\right.\)
Khối lượng hỗn hợp kim loại là:
\(m_{Mg}+m_{Al}=9+9=18\left(g\right)\)
Vậy ...
\(n_{H_2}=\dfrac{V}{22,4}=\dfrac{19,6}{22,4}=0,875\left(mol\right)\)
Đặt \(m_{Mg}=m_{Al}=a\left(g\right)\left(a>0\right)\)
\(\Rightarrow n_{Mg}=\dfrac{m}{M}=\dfrac{a}{24}\left(mol\right)\\ n_{Al}=\dfrac{m}{M}=\dfrac{a}{27}\left(mol\right)\)
\(pthh:Mg+HCl\rightarrow MgCl_2+H_2\left(1\right)\\ 2Al+6HCl\rightarrow2AlCl_3+3H_2\left(2\right)\)
Theo \(pthh\left(1\right):n_{H_2\left(1\right)}=n_{Al}=\dfrac{a}{24}\left(mol\right)\)
Theo \(pthh\left(1\right):n_{H_2\left(1\right)}=\dfrac{3}{2}n_{Al}=\dfrac{3}{2}\cdot\dfrac{a}{27}=\dfrac{a}{18}\left(mol\right)\)
\(\Rightarrow\Sigma n_{H_2}=n_{H_2\left(1\right)}+n_{H_2\left(2\right)}\\ \Rightarrow0,875=\dfrac{a}{24}+\dfrac{a}{18}\\ \Rightarrow\dfrac{7}{72}a=0,875=9\left(T/m\right)\)
\(m_{h^2}=2a=2\cdot9=18\left(g\right)\)

\(a,Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\\ n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ b,n_{Fe}=n_{H_2}=0,2\left(mol\right)\\ \%m_{Fe}=\dfrac{0,2.56}{12,8}.100\%=87,5\%\\ \%m_{Fe_2O_3}=100\%-87,5\%=12,5\%\\ c,n_{Fe_2O_3}=\dfrac{12,8-11,2}{160}=0,01\left(mol\right)\\ n_{H_2SO_4}=n_{Fe}+3n_{Fe_2O_3}=0,2+3.0,01=0,23\left(mol\right)\\ V_{ddH_2SO_4}=\dfrac{0,23}{0,46}=0,5\left(M\right)\)

\(n_{H_2}=\dfrac{2,24}{22,4}=0,1(mol)\\ Mg+2HCl\to MgCl_2+H_2\\ MgO+2HCl\to MgCl_2+H_2O\\ \Rightarrow n_{Mg}=0,1(mol)\\ \Rightarrow \%_{Mg}=\dfrac{0,1.24}{6,4}.100\%=37,5\%\\ \Rightarrow \%_{MgO}=100\%-37,5\%=62,5\%\)
\(b,n_{MgO}=\dfrac{6,4-0,1.24}{40}=0,1(mol)\\ \Rightarrow n_{HCl}=2.0,1+2.0,1=0,4(mol)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,4}{0,5}=0,8(l)\\ c,n_{MgCl_2}=0,1+0,1=0,2(mol)\\ \Rightarrow C_{M_{MgCl_2}}=\dfrac{0,2}{0,8}=0,25M\)

$n_{HCl} = 0,3(mol) ; n_{CO_2} = 0,05(mol)$
\(CO_3^{2-}+H^+\rightarrow HCO_3^-\)
0,25.......0,25..........................(mol)
\(HCO_3^-+H^+\text{→}CO_2+H_2O\)
0,05........0,05....0,05........................(mol)
Gọi $n_{Na_2CO_3} = a(mol) ; n_{K_2CO_3} = b(mol) \Rightarrow 106a + 138b = 31,3(1)$
Ta có :
$n_{CO_3^{2-}} = a + b = 0,25(2)$
Từ (1)(2) suy ra a = 0,1 ;b = 0,15
$m_{K_2CO_3} = 0,15.138 = 20,7(gam)$

a. \(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
0,25 ..... 0,5 ................... 0,25 (mol)
\(m_{Mg}=0,25.24=6\left(g\right)\)
\(\rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{6}{10}.100\%=60\%\\\%m_{MgO}=100\%-60\%=40\%\end{matrix}\right.\)
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
0,1 ....... 0,2 (mol)
\(n_{HCl}=0,25+0,1=0,35\left(mol\right)\)
\(C_M\left(HCl\right)=\dfrac{0,35}{0,1}=3,5\left(M\right)\)

a) \(Fe+2HCl->FeCl_2+H_2\) (1)
\(2M+2xHCl->2MCl_x+xH_2\) (2)
=> \(n_{HCl}=2.n_{H_2}=2.\dfrac{1,008}{22,4}=0,09\left(mol\right)\)
=> mHCl = 0,09.36,5 = 3,285 (g)
Theo ĐLBTKL: \(m_A+m_{HCl}=m_{Muối}+m_{H_2}\)
=> \(m_A=4,575+0,045.2-3,285=1,38\left(g\right)\)
b) Đặt số mol Fe, M là a, b
=> 56a + M.b = 1,38 (***)
(1)(2) => a+ 0,5bx = 0,045 (*)
\(\left\{{}\begin{matrix}\dfrac{46.n_{NO_2}+64.n_{SO_2}}{n_{NO_2}+n_{SO_2}}=50,5\\n_{NO_2}+n_{SO_2}=\dfrac{1,8816}{22,4}=0,084\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}n_{NO_2}=0,063\\n_{SO_2}=0,021\end{matrix}\right.\)
Fe0 - 3e --> Fe+3
a---->3a
M0 -xe --> M+x
b-->bx
N+5 +1e--> N+4
___0,063<-0,063
S+6 + 2e --> S+4
___0,042<-0,021
Bảo oàn e: 3a + bx = 0,105 (**)
(*)(**) => \(\left\{{}\begin{matrix}a=0,015\\bx=0,06=>b=\dfrac{0,06}{x}\end{matrix}\right.\)
(***) => 0,015.56 + \(M.\dfrac{0,06}{x}\) = 1,38
=> M = 9x (g/mol)
Xét x = 1 => M = 9(L)
Xét x = 2 => M = 18(L)
Xét x = 3 => M = 27(Al)
a) nCO2 = 0,1 mol
nCa(OH)2 = 0,1 mol
\(\dfrac{nCO2}{nCa\left(OH\right)2}=\dfrac{0,1}{0,1}=1\) => tạo ra muối CaCO3
CO2 (0,1) + Ca(OH)2 (0,1) -----> CaCO3 (0,1) + H2O
- Theo PTHH: nCaCO3 = 0,1 mol
=> mCaCO3 = 0,1 . 100 = 10 gam
b) nCO2 = 0,1 mol
nCa(OH)2 = 0,05 mol
\(\dfrac{nCO2}{nCa\left(OH\right)2}=\dfrac{0,1}{0,05}=2\) => tạo ra muối Ca(HCO3)2
2CO2 (0,1) + Ca(OH)2 (0,05) -----> Ca(HCO3)2 (0,05)
- Theo PTHH: nCa(HCO3)2 = 0,05 mol
=> mCa(HCO3)2 = 0,05 . 162 = 8,1 gam
c) nCO2 = 0,1 mol
nCa(OH)2 = 5/74 mol
\(\dfrac{nCO2}{nCa\left(OH\right)2}=\dfrac{0,1}{\dfrac{5}{74}}=1,48\) => tạo ra 2 muối Ca(HCO3)2 và CaCO3
- Đặt nCaCO3 = x mol và nCa(HCO3)2 = y mol
CO2 (x) + Ca(OH)2 (x) -----> CaCO3 (x) + H2O (1)
2CO2 (2y) + Ca(OH)2 (y) -----> Ca(HCO3)2 (y) (2)
- Theo PTHH (1,2): \(\left\{{}\begin{matrix}x+2y=0,1\\x+y=\dfrac{5}{74}\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}x=\dfrac{13}{370}\left(mol\right)\\y=\dfrac{6}{185}\left(mol\right)\end{matrix}\right.\)
=> mCaCO3 = 13/370 . 100 = 130/37 (gam)
=> mCa(HCO3)2 = 6/185 . 162 = 972/185 (gam)