hào tan 10g KNO3 vào 150g nước. Tính nồng độ % của dung dịch
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B
Số mol H2 = 0,1 mol
Phương trình phản ứng:
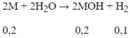
Tính được M = m : n = 7,8 : 0,2 = 39. Vậy kim loại cần tìm là K.
C M = 0 , 2 0 , 1 = 2 M

nMgO=\(\frac{12}{24+16}=0,3\) mol
mHCl = \(\frac{150.14,6}{100}=21,9\)g=> nHCl=\(\frac{21,9}{36,5}=0,6\) mol
PTHH: MgO+2HCl --> MgCl2+ H2O
0,3mol: 0,6mol----->0,3 mol--> ,0,3 mol
mMgCl2=0,3.( 24+35,5.2)=28,5g
theo định luật bảo toàn khối lượng
m MgCl2 =mMgO+mHCl-mH2O=12+150-0,3(1.2+16)=156,6 g
=> C% MgCl2\(=\frac{28,5}{156,6}.100=18,2\)%

\(m_{H_2SO_4}=\dfrac{14.150}{100}=21\left(g\right)\)

a) Pt: SO3 + H2O => H2SO4
b) nSO3 = \(\dfrac{8}{80}=0,1mol\)
Theo pt: nH2SO4 = nSO3 = 0,1 mol
=> CMH2SO4 = 0,1 : 0,25 = 0,4M

\(n_{Fe}=\dfrac{11.2}{56}=0.2\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(0.2.......0.4...................0.2\)
\(V_{H_2}=0.2\cdot22.4=4.48\left(l\right)\)
\(C_{M_{HCl}}=\dfrac{0.4}{0.4}=1\left(M\right)\)
\(n_{CuO}=\dfrac{8}{80}=0.1\left(mol\right)\)
\(CuO+H_2\underrightarrow{^{t^0}}Cu+H_2O\)
\(1............1\)
\(0.1.........0.2\)
\(LTL:\dfrac{0.1}{1}< \dfrac{0.2}{1}\Rightarrow H_2dư\)
\(n_{Cu}=n_{CuO}=0.1\left(mol\right)\)
\(m_{Cu}=0.1\cdot64=6.4\left(g\right)\)
Chúc em học tốt và có những trải nghiệm tuyệt vời tại hoc24.vn nhé !
a) nFe=0,2(mol)
PTHH: Fe + 2HCl -> FeCl2 + H2
0,2_________0,4____0,2___0,2(mol)
V(H2,dktc)=0,2.22,4=4,48(l)
b) VddHCl=0,4/0,4=1(l)
c) nCuO=0,1(mol)
PTHH: CuO + H2 -to-> Cu + H2O
Ta có: 0,2/1 > 0,1/1
=> CuO hết, H2 dư, tính theo nCuO
-> nCu=nCuO=0,1(mol)
=>mCu=0,1.64=6,4(g)
\(C\%_{dd}=\dfrac{10}{10+150}.100\%=6,25\%\)
m dd=10+150=160g
=>C%=10\160.100=6,25%