Cho 7,8g Zn vào dung dịch axit sunfuric loãng chứa 19,6g H2SO4
a) Tính VH2 thu được (ở đktc).Biết thể tích VH2 bị hao hụt là 5%
b) Còn dư bao nhiêu chất nào sau phản ứng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) 4Al : 4 nguyên tử Nhôm
b) $2Al(OH)_3$ : 2 phân tử Nhôm hidroxit
c) $3O_2$ : 3 phân tử oxi
d) $12C_6H_{12}O_6$ : 12 phân tử glucozo

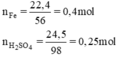
Phương trình hóa học của phản ứng:

So sánh tỉ lệ 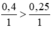 ⇒ Fe dư
⇒ Fe dư
Theo PT nFe (pư) = nH2SO4 = 0,25 mol ⇒ nFe dư = 0,4 – 0,25 = 0,15 mol
mFe dư = 0,15. 56 = 8,4g.
Do khối lượng Fe dư nên tính thể tích khí H2 theo số mol H2SO4.
nH2 = nH2SO4 = 0,25 mol
Vkhí = 0,25 . 22,4 = 5,6l.

a) nFe=0,4(mol); nH2SO4=0,5(mol)
PTHH: Fe + H2SO4 -> FeSO4 + H2
Ta có: 0,4/1 < 0,5/1
=> Fe hết, H2SO4 dư. tính theo nFe.
=> nH2= nH2SO4(p.ứ)=nFe=0,4(mol)
=>nH2SO4(dư)=0,5-0,4=0,1(mol)
=>H2SO4(dư)=0,1.98=9,8(g)
b) V(H2,dktc)=0,4.22,4=8,96(l)

PTHH: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\)
Ta có: \(\left\{{}\begin{matrix}n_{Zn}=\dfrac{26}{65}=0,4\left(mol\right)\\n_{H_2SO_4}=\dfrac{980\cdot10\%}{98}=1\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Axit còn dư, Kẽm p/ứ hết
\(\Rightarrow n_{H_2}=0,4\left(mol\right)\) \(\Rightarrow V_{H_2}=0,4\cdot22,4=8,96\left(l\right)\)

Chỉ có Zn phản ứng thôi. Cu không phản ứng, không tan.---->Chất rắn không tan là Cu
Zn+ H2SO4 ---> ZnSO4+ H2↑
0.1 0.1
nH2= 2.24: 22.4=0.1 mol
mZn= 0.1x65=6.5 g
mCu=10.5-6,5=4 g
%Zn=6.5:10.5x100%=61.9%
%Cu=4:10.5x100%=38.1%

a. PTHH :Fe + H2SO4 -> FeSO4 +H2
nFe = 22,4 : 56 = 0,4 (mol)
nH2SO4 = 24,5 : 98 = 0,25 (mol)
Ta có nFe > nH2SO4 (0,4>0,25) nên Fe dư
nFe dư = 0,4-0,25 = 0,15 (mol)
Vậy mFe dư = 0,15 . 56 = 8,4 (gam)
b, Theo PTHH ta có nH2 = nH2SO4 =0,25 (mol)
=> VH2 thu được (đktc) =0,25 . 22,4 =5,6(lit)
Ta có: \(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\\ n_{H_2SO_4\left(loãng\right)}=\dfrac{24,5}{98}=0,25\left(mol\right)\)
PTHH: Fe + H2SO4 (loãng) -> FeSO4 + H2\(\uparrow\)
Theo PTHH và đề bài, ta có:
\(\dfrac{n_{Fe\left(đềbài\right)}}{n_{Fe\left(PTHH\right)}}=\dfrac{0,4}{1}>\dfrac{n_{H_2SO_4\left(loãng,đềbài\right)}}{n_{H_2SO_4\left(loãng,PTHH\right)}}=\dfrac{0,25}{1}\)
=> H2SO4 loãng hết, Fe dư nên tính theo \(n_{H_2SO_4\left(loãng\right)}\)
Theo PTHH và đề bài, ta có:
\(n_{H_2}=n_{Fe\left(phảnứng\right)}=n_{H_2SO_4\left(loãng\right)}=0,25\left(mol\right)\\ =>n_{Fe\left(dư\right)}=0,4-0,25=0,15\left(mol\right)\)
a) Khối lượng Fe dư:
\(m_{Fe\left(dư\right)}=0,15.56=8,4\left(g\right)\)
b) Thể tích khí H2 thu được (ở đktc):
\(V_{H_2\left(đktc\right)}=0,25.22,4=5,6\left(l\right)\)

\(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right);n_{H_2SO_4}=\dfrac{24,5}{98}=0,25\left(mol\right)\\ PTHH:Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ Vì:\dfrac{0,4}{1}>\dfrac{0,25}{1}\Rightarrow Fe.dư\\ n_{H_2}=n_{Fe\left(p.ứ\right)}=n_{H_2SO_4}=0,25\left(mol\right)\\ a,V_{H_2\left(đktc\right)}=0,25.22,4=5,6\left(l\right)\\ b,n_{Fe\left(dư\right)}=0,4-0,25=0,15\left(g\right)\\ m_{Fe\left(dư\right)}=0,14.56=8,4\left(g\right)\)
nZn = 0,12 mol
nH2SO4 = 0,2 mol
Zn + H2SO4 → ZnSO4 + H2
Đặt tỉ lệ ta có
0,12 < 0,2
⇒ H2SO4 dư
⇒ mH2SO4 dư = ( 0,2 - 0,12 ).98 = 7,84 (g)
⇒ VH2 = 0,12.22,4.5% = 0,1344 (l)
cảm ơn bạn nhé thanks