cho 18,3 g hỗn hợp 2 kim loại A có hóa trị I và B có hóa trị II hòa tan hoàn toàn trong nước sau phản ứng có 25,1 g bazo tạo thành và V lít khí ở đktc . tính V lít ở đktc
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Nếu A không có K:
\(\%m_K=\dfrac{10,66}{29,34+10,66}\cdot100\%=26,65\%\ne29,35\%\\ R:Kali\\ K+H_2O->KOH+\dfrac{1}{2}H_2\\ M+2H_2O->M\left(OH\right)_2+H_2\\ n_K=a,n_M=b\left(mol\right)\\ n_{H_2}=0,5a+b=\dfrac{5,376}{22,4}=0,24mol\\ \%m_{K\left(B\right)}=\dfrac{39a+10,66}{29,34+10,66}\cdot100=29,35\\ a=0,028\\ b=0,226\\ M_M=\dfrac{29,34-39\cdot0,028}{0,226}=125\left(g\cdot mol^{^{-1}}\right)\)
Vậy không có kim loại kiềm thổ thoả đề

\(Gọi\ n_{H_2} = n_{H_2SO_4} = a(mol)\)
Bảo toàn khối lượng :
\(30,5 + 98a = 2a + 97,7\\ \Rightarrow a = 0,7(mol)\\ \Rightarrow V = 0,7.22,4 = 15,68(lít)\)

Chuyển đổi hết từ khối lượng chất sang mol chất, rồi viết phương trình phản ứng , tính từng bước theo phương trình hóa học sẽ ra được.

Phản ứng tổng quát:
\(R_2\left(CO_3\right)_n+2nHCl->2RCl_n+nCO_2+nH_2O\)
hay:
\(CO_3^{^{ }2-}+2H^{^{ }+}->CO_2+H_2O\\ n_{CO_2}=\dfrac{0,896}{22,4}=0,04mol=n_{CO_3^{^{ }2-}}\\ n_{H^{^{ }+}}=0,08=n_{HCl}=n_{Cl^{^{ }-}}\\ m_{muối}=3,34-60.0,04+0,08.35,5=3,78g\)

a, Ozon có thể oxi hóa bạc. Ozon phản ứng với KI
b, Theo gt ta có: $n_{H_2}=0,6(mol)$
Vì M có hóa trị II nên ta có: $n_{hh}=0,6(mol)$
Suy ra $M_{tb}=11,5$. Vô lý
Do đó M không bị hòa tan. $\Rightarrow n_{Mg}=0,6(mol)\Rightarrow m_{M}=-7,5(g)$ Vô lý.
Bạn kiểm tra đề nhé!

Đáp án C
Gọi công thức của hai muối trong hỗn hợp ban đầu là A2CO3 và BCO3.
Có các phản ứng:
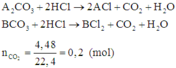
Quan sát phản ứng thấy khi cho hỗn hợp phản ứng với dung dịch HCl thì mỗi gốc C O 3 2 - trong muối được thay thế bởi hai gốc Cl-.
Có 1 mol C O 3 2 - bị thay thế bởi 2 mol Cl- thì khối lượng của muối tăng: (2.35,5 -60) = 11(gam)
Do đó khối lượng muối khan thu được khi cô cạn dung dịch là:
mmuối clorua = mmuối cacbonat + 0,2.11 = 23,8 + 0,2.11= 26 (gam)

Câu 3
Theo ĐLBTKL: mhh(ban đầu) = mhh(sau pư) + mCO2
=> mCO2 = 1,3 - 0,8 = 0,5 (g)
=> \(n_{CO_2}=\dfrac{0,5}{44}=\dfrac{1}{88}\left(mol\right)\)
=> \(V_{CO_2}=\dfrac{1}{88}.22,4=0,255\left(l\right)\)
Câu 4:
\(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH: A + 2HCl --> ACl2 + H2
____0,5<---------------------0,5
=> \(M_A=\dfrac{12}{0,5}=24\left(g/mol\right)=>Mg\)


