hòa tan hoàn toàn 35g hỗn hợp gồm Mg,Al,Zn vào dung dịch HCl dư thấy thoát ra 19,04l H2 ở đktc.biết thể tích khí H2 thoát ra do Al phản ứng gấp 2 lần thể tích khí H2 thoát ra do Mg phản ứng
a, viết các pthh xảy ra
b, tính kl mỗi kim loại trong hỗn hợp ban đầu
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH: Mg + 2HCl → MgCl2 + H2 ↑
Fe + 2HCl → FeCl2 + H2 ↑
2Al + 6HCl → 2AlCl3 + 3H2 ↑
Gọi số mol của H2 thoát ra do Al là 2a => số mol H2 thoát ra do Mg là a (Vì thể tích tỉ lệ thuận vs số mol) , Số mol H2 do Fe thoát ra là b.
Số mol của H2 là: 17,04 : 22,4 = 0,761 mol
Ta có hệ pt:
- 24a + 56b + 27.2a = 31,4
- a + b + 3a = 0,761
- => a = 0.077 ; b = 0,4535
Khối lượng Fe là: 56b = 56 . 0,4535 = 25,4 gam
Khối lượng Mg là: 24a = 1,85 gam
Khối lượng Al là: 27 . 2a = 4,15 gam

A tác dụng với nước
\(n_{H_2}=\dfrac{3,7185}{24,79}=0,15mol\\ Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\)
\(a----------\rightarrow a\)
\(Ba\left(OH\right)_2+2Al+2H_2O\rightarrow Ba\left(AlO_2\right)_2+3H_2\)
\(a----------------\rightarrow3a\)
\(\Rightarrow a+3a=0,15\\ \Rightarrow a=0,0375mol\)
A tác dụng với NaOH
\(n_{H_2}=\dfrac{7,347}{24,79}=0,3mol\)
\(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\)
\(a----------\rightarrow a\)
\(2Al+2NaOH+2H_2O\rightarrow2NaAlO_2+3H_2\)
\(b---------------\rightarrow1,5b\)
\(\Rightarrow a+1,5b=0,3\\ \Rightarrow0,0375+1,5b=0,3\\ \Rightarrow b=0,175mol\)
A tác dụng với HCl
\(n_{H_2}=\dfrac{9,916}{24,79}=0,4mol\)
\(Ba+2HCl\rightarrow BaCl_2+H_2\)
\(a---------\rightarrow a\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(b---------\rightarrow1,5b\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(c---------\rightarrow c\)
\(\Rightarrow a+1,5b+c=0,4\\ \Rightarrow0,0375+1,5.0,175+c=0,4\\ \Rightarrow c=0,1mol\)
\(m_A=0,0375.137+0,175.27+0,1.24=12,2625g\\ \%m_{Ba}=\dfrac{0,0375.137}{12,2625}\cdot100=41,9\%\\ \%m_{Al}=\dfrac{0,175.27}{12,2625}\cdot100=38,53\%\\ \%m_{Mg}=100-41,9-38,53=19,57\%\)

Gọi \(n_{H_2\left(Mg\right)}=a\left(mol\right)\rightarrow n_{H_2\left(Al\right)}=2a\left(mol\right)\)
PTHH:
2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2
\(\dfrac{4a}{3}\) 2a
Mg + H2SO4 ---> MgSO4 + H2
a a
\(m_{Al}=\dfrac{4a}{3}.27=36a\left(g\right)\\ \rightarrow V_{Mg}=V_{Al}=\dfrac{36a}{2,7}=\dfrac{40a}{3}\left(cm^3\right)\)
\(m_{Mg}=24a\left(g\right)\\ \rightarrow D_{Mg}=\dfrac{24a}{\dfrac{40}{3}}=1,8\left(\dfrac{g}{cm^3}\right)\)

\(Đặt:\)
\(\left\{{}\begin{matrix}n_{Mg}=x\left(mol\right)\\\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
\(n_{H_2}=\dfrac{6.72}{22.4}=0.3\left(mol\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\\ Fe+2HCl\rightarrow FeCl_2+H_2\)
\(m_{hh}=24x+56y=13.6\left(g\right)\\ n_{H_2}=x+y=0.3\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}x=0.1\\y=0.2\end{matrix}\right.\)
\(\%Mg=\dfrac{0.1\cdot24}{13.6}\cdot100\%=17.64\%\\ \%Fe=100-17.64=82.36\%\)
\(n_{HCl}=2n_{H_2}=2\cdot0.3=0.6\left(mol\right)\)
\(V_{HCl}=\dfrac{0.6}{2}=0.3\left(l\right)\)
\(m_Y=m_{MgCl_2}+m_{FeCl_2}=0.1\cdot95+0.2\cdot127=34.9\left(g\right)\)

HD:
Thí nghiệm 1 chỉ có Na phản ứng:
Na + HOH \(\rightarrow\) NaOH + 1/2H2 (1)
0,4 0,2 mol
Thí nghiệm 2 chỉ có Al phản ứng (kim loại lưỡng tính):
Al + OH- + H2O \(\rightarrow\) AlO2- + 3/2H2 (2)
0,7/3 0,35 mol
Thí nghiệm 3 cả 3 chất đều phản ứng:
2Na + H2SO4 \(\rightarrow\) Na2SO4 + H2 (3)
Mg + H2SO4 \(\rightarrow\) MgSO4 + H2 (4)
2Al + 3H2SO4 \(\rightarrow\) Al2(SO4)3 + 3H2 (5)
Gọi x, y, z tương ứng là số mol của Na, Mg và Al trong a gam hh.
Ta có: x = 0,4 mol; z = 0,7/3 mol; x/2 + y + 3z/2 = 0,5. Suy ra: y = -0.5 < 0 (vô lí)
Bạn xem lại đề bài, đề bài ko đúng.

Đáp án D
n H 2 = 0 , 5 mol
Cu là kim loại đứng sau hidro trong dãy hoạt động hoá học, do đó Cu không tác dụng với dung dịch HCl
Sơ đồ phản ứng:
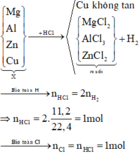
Khối lượng muối chính là khối lượng kim loại Mg, Al, Zn và Cl. Khi đó ta có:
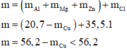
Chỉ có 49,80 < 56,2. Vậy giá trị của m có thể là 49,80 gam
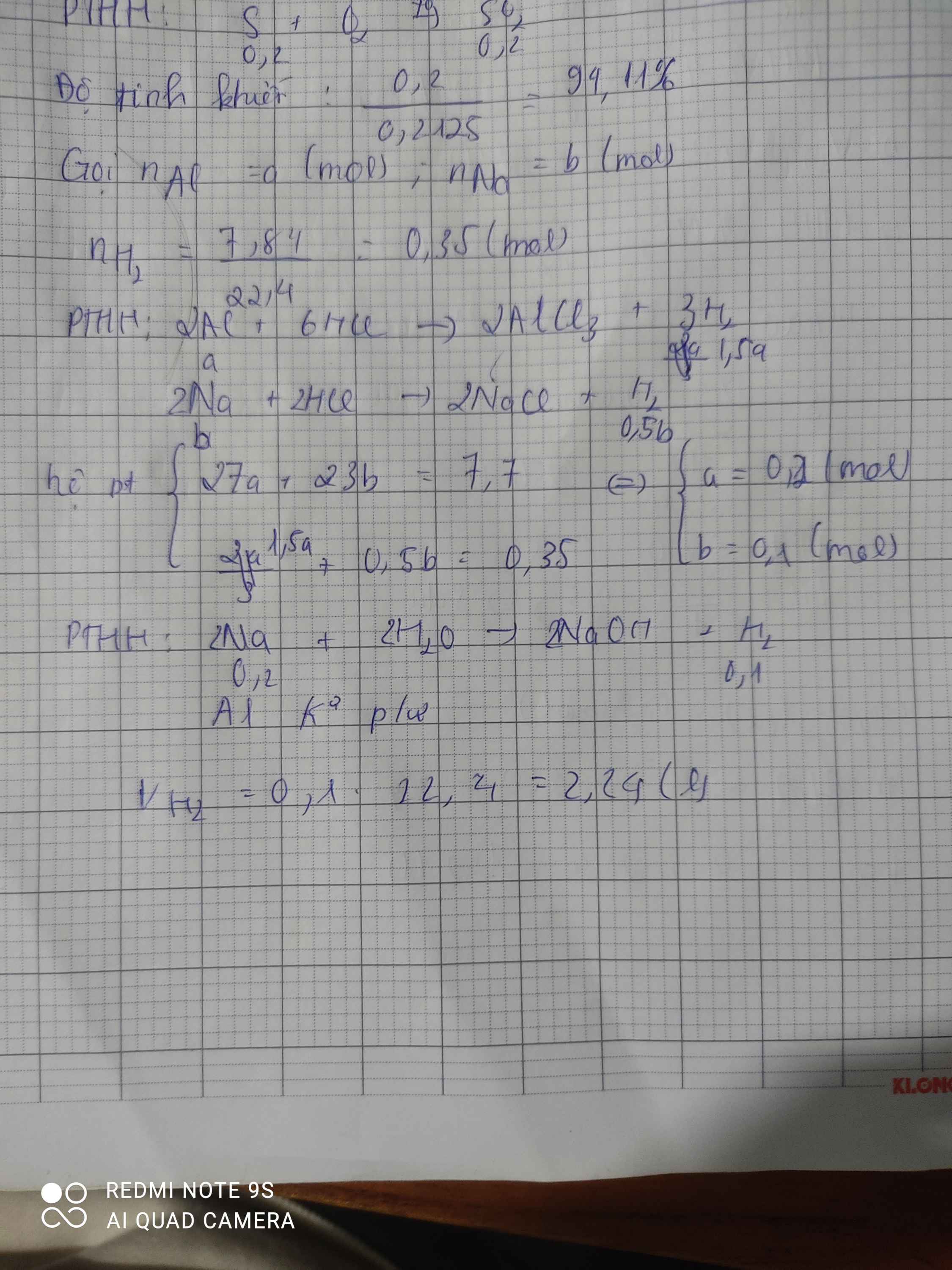
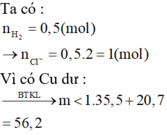

nHCl=19,04/22,4=0,85(mol)
Mg+2HCl--->MgCl2+H2
x_____2x_____x_____x
2Al+6HCl--->2AlCl3+3H2
y____3y_____y_______3/2y
Zn+2HCl--->ZnCl2+H2
1/2y__1/4y___1/2y___1/2y
Hệ pt:
\(\left\{{}\begin{matrix}24x+92y=35\\x+2y=0,85\end{matrix}\right.\)
=>x,y
=>mAl,Fe,Mg