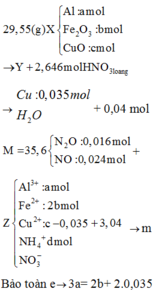cho m gam hỗn hợp gồm cu, fe, al tác dụng hoàn toàn với dd HNO3 loãng được [m+31] g muối nitrat nếu cho m gam hộn hợp kim loại trên tác dụng với o2 được các õit cuo ,fe2o3 al2o3 thì khối lượng m của oxit là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ta có: mNO3-= mmuối nitrat- mkim loại= (m+31)-m= 31 gam → nNO3-= 0,5 mol
Ta thấy số oxi hóa của Cu, Fe, Al trong muối nitrat và trong các oxit tương ứng là bằng nhau
→nNO3-= nđiện tích dương của cation= 2.nO2- → nO2-= 0,25 mol
→ moxit= mkim loại+ mO2-= m+ 0,25.16= m+ 4 (gam)
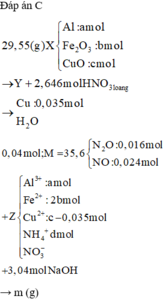
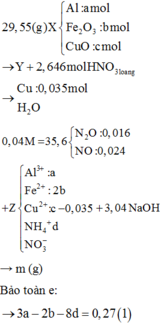
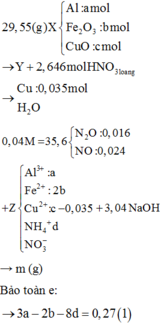
Đáp án C

m O/oxit = m giảm = 44,2 – 33,8 = 10,4g
nO =10,4:16 = 0,65
Xét toàn bộ quá trình ta có: số oxi hóa của kim loại không đổi
⇒ ne = 2nO = 1,3 mol
Có nNO3-/muối = ne = 1,3
m muối = mNO3- + mKL = 33,8 + 1,3.62 = 114,4g
Đáp án B.

a)
$2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
$Cu + 4HNO_3 \to Cu(NO_3)_2 + 2NO_2 + 2H_2O$
n H2 = 16,8/22,4 = 0,75(mol)
Theo PTHH :
n Al = 2/3 n H2 = 0,5(mol)
n NO2 = 44,8/22,4 = 2(mol)
Theo PTHH :
n Cu = 1/2 n NO2 = 1(mol)
Suy ra :
m = 0,5.27 + 1.64 = 77,5(gam)
TH2 : Nếu axit HNO3 đã dùng là axit đặc nóng
$2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
$Cu + 4HNO_3 \to Cu(NO_3)_2 + 2NO_2 + 2H_2O$
$Al + 6HNO_3 \to Al(NO_3)_3 + 3NO_2 + 3H_2O$
n H2 = 16,8/22,4 = 0,75(mol)
n NO2 = 44,8/22,4 = 2(mol)
Theo PTHH :
n Al = 2/3 n H2 = 0,75.2/3 = 0,5(mol)
n NO2 = 2n Cu + 3n Al = 2n Cu + 0,5.3 = 2(mol)
=> n Cu = 0,25(mol)
Suy ra :
m = 0,5.27 + 0,25.64 = 29,5 gam

Đáp án D
Đặt Zn, Cr,Sn là x mol → ZnCl2 : x mol, SnCl2 : x mol và CrCl2 : x mol
→ x =0,02 mol
Bảo toàn O trong phương trình đốt cháy có 2nO2 = x + 2x + 3/2 x =0,09
→ VO2= 1,008 lít