đốt cháy hoàn toàn 18 gam FeS2. hấp thụ toàn bộ lượng SO2 thu được cần 2 lít dung dịch Ba(OH)2 0,125M. Tính khối lượng muối tạo thành
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
![]()
Vì ![]() nên chỉ có hai trường hợp là SO2 thiếu hoặc phản ứng tạo hai muối. Đề bài yêu cầu tìm giá trị lớn nhất của m nên khi cho SO2 vào dung dịch X sẽ tạo hai muối
H
S
O
-
3
và
S
O
2
-
3
nên chỉ có hai trường hợp là SO2 thiếu hoặc phản ứng tạo hai muối. Đề bài yêu cầu tìm giá trị lớn nhất của m nên khi cho SO2 vào dung dịch X sẽ tạo hai muối
H
S
O
-
3
và
S
O
2
-
3
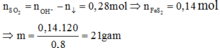

Đáp án C
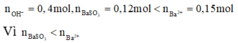
nên chỉ có hai trường hợp là SO2 thiếu hoặc phản ứng tạo hai muối. Đề bài yêu cầu tìm giá trị lớn nhất của m nên khi cho SO2 vào dung dịch


\(n_{BaSO_3}=\dfrac{21.7}{217}=0.1\left(mol\right)\)
\(BTBa:\)
\(n_{Ba\left(HSO_3\right)_2}=0.2\cdot0.75-0.1=0.05\left(mol\right)\)
\(BTS:\)
\(n_{FeS_2}=\dfrac{0.1+0.05\cdot2}{2}=0.1\left(mol\right)\)
\(m_{FeS_2}=0.1\cdot120=12\left(g\right)\)
$n_{Ba(OH)_2} = 0,2.0,75 = 0,15(mol)$
$n_{BaSO_3} = 0,1(mol)$
TH1: $Ba(OH)_2$ dư
Ba(OH)2 + SO2 → BaSO3 + H2O
0,1..............0,1.........0,1........................(mol)
Bảo toàn nguyên tố với S :
$n_{FeS_2} = \dfrac{1}{2}n_{SO_2} = 0,05(mol)$
$m = 0,05.120 = 6(gam)$
TH2 : Có tạo muối axit
Ba(OH)2 + SO2 → BaSO3 + H2O
0,1..............0,1.........0,1........................(mol)
Ba(OH)2 + 2SO2 → Ba(HSO3)2
0,05.............0,1........................................(mol)
$n_{SO_2} = 0,2(mol)$
$n_{FeS_2} = \dfrac{1}{2}n_{SO_2} = 0,1(mol)$
$m = 0,1.120 = 12(gam)$

\(4FeS_2+11O_2\rightarrow\left(t^o\right)2Fe_2O_3+8SO_2\) (1)
\(n_{Ba\left(OH\right)_2}=0,2.1=0,2\left(mol\right)\)
\(n_{BaSO_3}=\dfrac{32,55}{217}=0,15\left(mol\right)\)
`@`TH1: Chỉ tạo ra kết tủa
\(Ba\left(OH\right)_2+SO_2\rightarrow BaSO_3\downarrow+H_2O\)
0,15 0,15 ( mol )
Theo ptr (1): \(n_{FeS_2}=\dfrac{n_{SO_2}}{2}=\dfrac{0,15}{2}=0,075\left(mol\right)\)
\(m_{FeS_2}=0,075.120=9\left(g\right)\)
`@` TH2: Ba(OH)2 hết
\(Ba\left(OH\right)_2+SO_2\rightarrow BaSO_3\downarrow+H_2O\)
0,2 ( mol )
0,15 0,15 0,15 ( mol )
\(Ba\left(OH\right)_2+2SO_2\rightarrow Ba\left(HSO_3\right)_2\)
0,05 0,1 ( mol )
Theo ptr (1): \(n_{FeS_2}=\dfrac{n_{SO_2}}{2}=\dfrac{0,15+0,1}{2}=0,125\left(mol\right)\)
\(n_{FeS_2}=0,125.120=15\left(g\right)\)

Đáp án : D
Amino axit CnH2n+1O2N
X : C5nH10n-3O6N5 ; Y : C6nH12n-4O7N6
, nCO2 = nBaCO3 = 1,5 mol = 0,1.5 => n = 3
Xét TN2 : 0,15 mol Y + NaOH
=> muối là : C3H6O2NNa : 0,15.6 = 0,9 mol
=> m = 99,9g
. Phương trình hóa học 4FeS2 + 11O2 => 2Fe2O3 + 8SO2
nFeS2 = 18/120 = 0,15 mol => nSO2 = 0,3 mol
nBa(OH)2 = 0,25 mol. Như vậy trường hợp này tạo hai muối.
Gọi x, y lần lượt là số mol muối trung hòa và axit.
Có hệ phương trình về số mol của Ba(OH)2 và SO2 là:
x + y = 0,25 và x + 2y = 0,3
Giải hệ PT được: x = 0,2 và y = 0,05
=> Khối lượng muối là m = 0,2.197 + 0,05.259 = 52,35 gam