Cho 2,6 gam Kẽm tác dụng vừa đủ với axit clohiđric theo sơ đồ phản ứng sau:
Zn + HCl ----> ZnCl2 + H2
a) Lập phương trình phản ứng trên.
b) Tính thể tích khí H2 thoát ra (đktc).
c) Tính khối lượng axit clohiđric (HCl) đã dùng cho phản ứng trên.
d) Tính số phân tử Zn đã phản ứng.




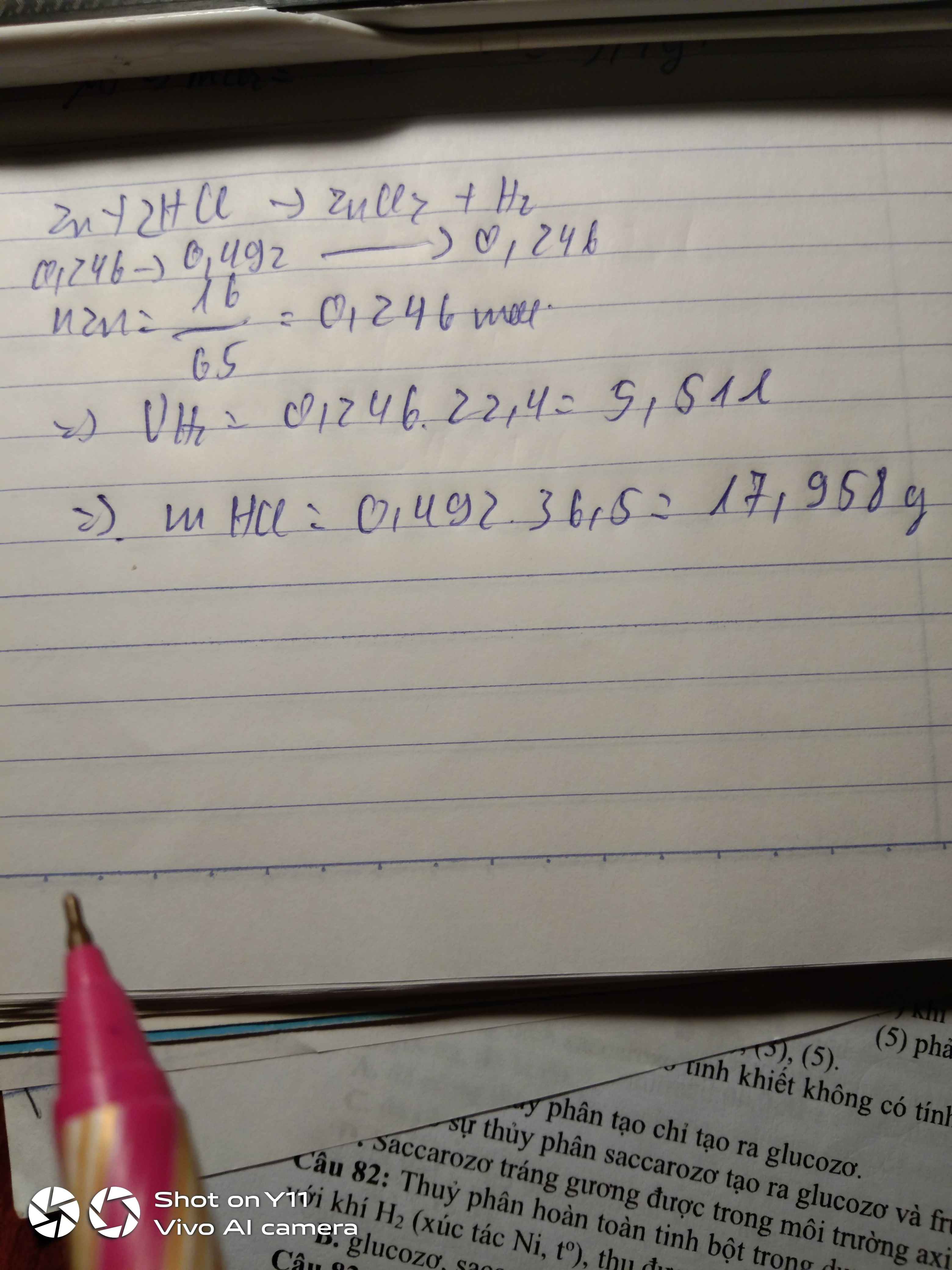
a)PTHH:
Zn + 2HCl \(\rightarrow\) ZnCl2 + H2
a)Số mol của kẽm:
\(n_{Zn}=\dfrac{2,6}{65}=0,04\left(mol\right)\)
PTHH:
Zn + 2HCl \(\rightarrow\) ZnCl2 + H2
1mol 2mol 1mol 1mol
0,04mol 0,08mol 0,04mol 0,04mol
b)Thể tích khí H2 thoát ra ở (đktc):
\(V_{H_2}=0,04.22,4=0,896\left(l\right)\)
c)Khối lượng HCl đã dùng;
\(m_{HCl}=0,08.36,5=2,92\left(g\right)\)
d)Số phân tử Zn đã phản ứng:
\(A_{Zn}=0,04.6.10^{23}=2,4.10^{22}\)(phân tử)
a.Zn+2HCl----->ZnCl2+H2
b.\(n_{Zn}=\dfrac{m_{Zn}}{M_{Zn}}=\dfrac{2,6}{65}=0,04\left(mol\right)\)
Theo PTPỨ:\(n_{H_2}=n_{Zn}=0,04\left(mol\right)\)
\(V_{H_2}=n_{H_2}.22,4=0,04.22,4=0,896\left(l\right)\)
c.Theo PTPỨ:\(n_{HCl}=2n_{Zn}=2.0,04=0,08\left(mol\right)\)
\(m_{HCl}=n_{HCl}.M_{HCl}=0,08.36,5=2,92\left(g\right)\)
d.Số phân tử Zn:\(n_{Zn}.6.10^{23}=0,04.6.10^{23}=0,24.10^{23}\left(phântử\right)\)
Chúc bạn học tốt