Cho 7,2g hỗn hợp A gồm fe và FexOy tan hết trong dung dịch HCl 1M dư thu được 0,56 lít khí H2 ở đktc và dung dịch B.Cho toàn bộ dung dịch B vào NaOH dư đun xôi trong điều kiện có không khí lọc lấy kết tủa rửa sách nung nóng đến khối lượng không đổi thu được 8g chất rắn
a) Xác định thành phần % khối lượng mỗi kim loại trong hỗn hợp A
b) Tím công thức oxit sắt
c) Tính thể tích HCl dư

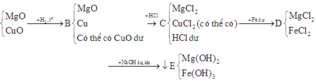
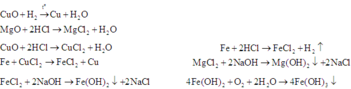

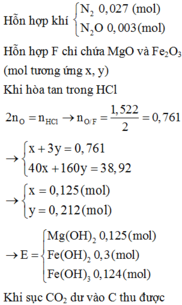





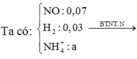
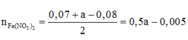
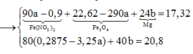
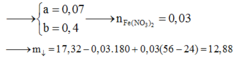
Fe + 2HCl -> FeCl2 + H2 (1)
FexOy + 2yHCl -> xFeCl2y/x + yH2O (2)
nH2=0,025(mol)
nFe2O3=0,05(mol)
Ta có:
nFe=2nFe2O3=0,1(mol)
mFe trong Fe;FexOy=56.0,1=5,6(g)
mFe trong A=nH2=0,025(mol)
mFe trong A=0,025.56=1,4(g)
mFexOy=7,2-1,4=5,8(g)
mFe trong FexOy=5,6-1,4=4,2(g)
mO trong FexOy=7,2-5,6=1,6(g)
nFe trong FexOy=0,075(mol)
nO trong FexOy=0,1(mol)
=>\(\dfrac{x}{y}=\dfrac{0,075}{0,1}=\dfrac{3}{4}\)
Vậy CTHH của oxit sắt là Fe3O4