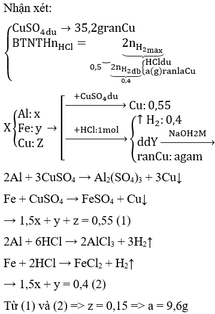
Cho 26,91 g kim loại M vào 700 ml dung dịch AlCl3 0,5M sau khi phản ứng xảy ra hoàn toàn thu được V lít khí H2 (đktc) và 17,94 g kết tủa . Xác định kim loại M và giá trị của V
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


M là kim loại hóa trị 1, cho M vào dung dịch AlCl3 thu được khí H2 và kết tủa
=> M là kim loại kiềm
\(M+H_2O\rightarrow MOH+\dfrac{1}{2}H_2\) (1)
\(3MOH+AlCl_3\rightarrow Al\left(OH\right)_3+3NaCl\) (2)
\(n_{Al\left(OH\right)_3}=\dfrac{26,91}{78}=0,345\left(mol\right)\)
\(n_{AlCl_3}=0,7.0,75=0,525\left(mol\right)\)
Vì \(n_{Al\left(OH\right)_3}< n_{AlCl_3}\) nên:
TH1: AlCl3 phản ứng hết và kết tủa tan 1 phần trong MOH
Al(OH)3 + MOH → MAlO2 + 2H2O (3)
Bảo toàn nguyên tố Al => \(n_{MAlO_2}=0,525-0,345=0,18\left(mol\right)\)
Theo (3) : \(n_{MAlO_2}=n_{MOH}=0,18\left(mol\right)\)
Theo (2) : \(n_{MOH}=3n_{AlCl_3}=0,525.3=1,575\left(mol\right)\)
=> \(\Sigma n_{MOH}=1,575+0,18=1,755\left(mol\right)\)
Theo (1) : \(n_M=n_{MOH}=1,755\left(mol\right)\)
=> \(M_M=\dfrac{4,365}{1,755}=2,49\left(loại\right)\)
TH2: AlCl3 còn dư, MOH phản ứng hết
Theo (2) => \(n_{MOH}=3n_{Al\left(OH\right)_3}=1,035\left(mol\right)\)
Theo (1) => \(n_M=n_{MOH}=1,035\left(mol\right)\)
=> \(M_M=\dfrac{4,365}{1,035}=4,2\left(loại\right)\)
Bạn xem lại đề giúp mình nhé

Câu 3. Hòa tan 16,2 g hh kim loại kiềm và oxit của nó thu được V lít H2 ( đktc) ,lấy dd sau pư cho vào 50 ml dd AlCl3 0,5 M ,sau khi pư xẩy ra hoàn toàn thu được 15,6 gm kết tủa .xác định M

Chọn đáp án B
nH2 = 0,15 ⇒ nOH- = 0,3 mà nAl3+ = 0,2.0,4 = 0,08 > 0,3/4 Al chỉ mới tan 1 phần
Ta có 4nAl(OH)4- + 3nAl(OH)3 = 0,3 mà nAl(OH)4- + nAl(OH)3 = 0,08
⇒ nAl(OH)3 .
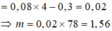

Chọn đáp án B
nH2 = 0,15 ⇒ nOH- = 0,3 mà nAl3+ = 0,2.0,4 = 0,08 > 0,3/4 Al chỉ mới tan 1 phần
Ta có 4nAl(OH)4- + 3nAl(OH)3 = 0,3 mà nAl(OH)4- + nAl(OH)3 = 0,08
⇒ nAl(OH)3 .
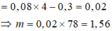

Đáp án C
nZn = nH2 = 0,2 => m = mZn + mCu = 0,2.65 +2 = 15 => Chọn C.

Đáp án C
nZn = nH2 = 0,2 => m = mZn + mCu = 0,2.65 +2 = 15 => Chọn C.