Cho 9,8g 1 hidroxit của kim loại hóa trị II và tác dụng vừa đủ với 7,3g HCl. XĐ CTHH của hidroxit trên
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{HCl}=\dfrac{146\cdot10\%}{36.5}=0.4\left(mol\right)\)
\(M\left(OH\right)_2+2HCl\rightarrow MCl_2+2H_2O\)
\(0.2...............0.4\)
\(M_{M\left(OH\right)_2}=\dfrac{11.6}{0.2}=58\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow M+34=58\)
\(\Rightarrow M=24\)
\(M:Mg\left(Magie\right)\)

\(n_{H_2SO_4}=\dfrac{25,8}{98}=\dfrac{129}{490}mol\)
\(2R\left(OH\right)_3+3H_2SO_4\rightarrow R_2\left(SO_4\right)_3+6H_2O\)
\(\dfrac{43}{245}\) \(\leftarrow\) \(\dfrac{129}{490}\)
\(\Rightarrow M_{R\left(OH\right)_3}=\dfrac{18,9}{\dfrac{43}{245}}\approx107\)
\(\Rightarrow M_R+3\cdot17=107\Rightarrow M_R=56\)
\(\Rightarrow R\) là sắt Fe.
CTHH của hidroxit là \(Fe\left(OH\right)_3\) có tên sắt (lll) hidroxit.
Cho 18g 1 bazo của kim loại R Hóa trị II tác dụng vừa đủ vs 400ml dd HCl 1M. Hãy tìm kim loại R trên

\(n_{HCl}=0,4.1=0,4\left(mol\right)\)
PT: \(R\left(OH\right)_2+2HCl\rightarrow RCl_2+2H_2O\)
Theo PT: \(n_{R\left(OH\right)_2}=\dfrac{1}{2}n_{HCl}=0,2\left(mol\right)\)
\(\Rightarrow M_{R\left(OH\right)_2}=\dfrac{18}{0,2}=90\left(g/mol\right)\)
\(\Rightarrow M_R+34=90\Rightarrow M_R=56\left(g/mol\right)\)
→ R là Fe.

a) Gọi công thức hidroxit cần tìm là M(OH)x
nHCl = 0,2 mol
xHCl + M(OH)x ➝ MClx + xH2O
0,2------\(\frac{0,2}{x}\)
=> \(\frac{0,2}{x}\) = \(\frac{9,8}{M+17x}\)
Vì M là kim loại nên x∈ \(\left\{1;2;3\right\}\)
Thay các giá trị vào ta có x = 2 thõa mãn và M = 64 => M là Cu
b) Cu(OH)2 ➝ CuO + H2O
nCuO = nCu(OH)2 = 0,1 mol
=> mCuO = 8 g
=> Khối lượng CuO thực tế thu được là : m= 7,2 g

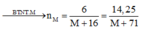
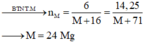
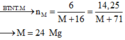
Gọi CTHH của hidroxit là X(OH)2
X(OH)2 + 2HCl -> XCl2 + 2H2O
nHCl=0,2(mol)
Theo PTHH ta có:
nX(OH)2=\(\dfrac{1}{2}\)nHCl=0,1(mol)
MX(OH)2=9,8:0,1=98
MX=98-17.2=64
Vậy X là đồng,KHHH là Cu
CTHH của hidroxit là Cu(OH)2