1. Dẫn 10 lít hỗn hợp khí A (đktc) gồm O2, CO2 đi qua dung dịch có chứa 0,2 mol Ca(OH)2. Sau phản ứng thu được 1g kết tủa. Tính % thể tích của hỗn hợp A.
2. Cho V lít CO2 (đktc) vào 200ml dung dịch Ca(OH)2 2M. Sau phản ứng được 30g kết tủa. Tính V?
3. Cho 0,5 mol hỗn hợp A gồm CO2, SO2 có dA/O2 = 1,75 vào 0,375 lít dung dịch Ba(OH)21M. Tính tổng khối lượng muối thu được sau phản ứng.
P/s: Em xin lỗi nhưng nếu anh/chị nào làm được thì có thể ghi rõ cả bài giải ra giùm em nha.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nCa(OH)2 = 2.0,01 = 0,02 (mol)
\(n_{CaCO_3}=\dfrac{1}{100}=0,01\left(mol\right)\)
TH1: Nếu kết tủa không bị hòa tan
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
0,01<----0,01
=> \(\left\{{}\begin{matrix}V_{CO_2}=0,01.22,4=0,224\left(l\right)\\V_{N_2}=1-0,224=0,776\left(l\right)\end{matrix}\right.\)
TH2: Nếu kết tủa bị hòa tan 1 phần
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
0,02---->0,02------>0,02
CaCO3 + CO2 + H2O --> Ca(HCO3)2
0,01--->0,01
=> VCO2 = (0,02 + 0,01).22,4 = 0,672 (l)
=> VN2 = 1 - 0,672 = 0,328 (l)

Số mol Ca(OH)2 = 2.0,02 = 0,04 mol
Số mol Ca(OH)2 = 2.0,02 = 0,04 mol
Số mol CaCO3 = 1_100=0,01 mol
Bài toán này có thể là 1 trong 2 trường hợp sau:
TH1: Số mol CO2 không đủ tác dụng với số mol Ca(OH)2
CO2 + Ca(OH)2 → CaCO3↓ + H2O
Số mol CO2 = số mol CaCO3 =0,01 mol
=>Thể tích CO2 = 22,4.0,01=0,224 lít
Vậy %thể tích CO2 = (0,224.100)/10=2,24%
TH2: Số mol CO2 nhiều hơn số mol Ca(OH)2 tham gia phản ứng:
CO2 + Ca(OH)2 → CaCO3↓ + H2O (1)
CaCO3 + CO2 + H2O → Ca(HCO3)2 (2)
Theo (1): số mol CO2 (1) = số mol CaCO3 = Số mol Ca(OH)2 = 0,04 mol
Ta có: Số mol CaCO3 (2) = 0,04-0,01 = 0,03 (mol)
Theo (2): Số mol CO2(2) = số mol CaCO3 (2) = 0,03 (mol)
Vậy tổng số mol CO2 phản ứng (1) và (2) là 0,04 + 0,03 = 0,07 mol
Do đó %thể tích CO2 = (0,07.22,4.100)/10 = 15,68%

Phương pháp:
- Tính số mol CO và H2.
- m↓ - mCO2 = m dung dịch giảm => mCO2
- Viết PTHH. Tính toán theo PTHH.
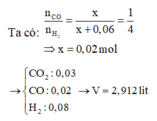
Đáp án C

Đáp án C
- Khi X + Ca(OH)2 thì chỉ có CO2 phản ứng:
=> mdung dịch giảm = mCaCO3 – mCO2 => mCO2 = 2 – 0,68 = 1,32g
=> nCO2 = 1,32: 44 = 0,03 mol
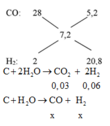
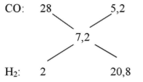
- Xét phản ứng ban đầu:
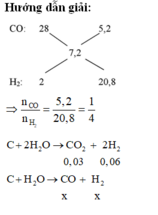
C + H2O → CO + H2
Mol x → x → x
C +2H2O → CO2 + 2H2
Mol 0,03 → 0,06
Vậy hỗn hợp khí cuối cùng gồm: x mol CO và (x + 0,06) mol H2
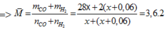
=> x = 0,02 mol
nKhí bđ = nCO2 + nCO + nH2 = 0,03 + 0,02 + 0,08 = 0,13 mol
=> Vkhí = 0,13.22,4 = 2,912 lit

Đáp án C
- Khi X + Ca(OH)2 thì chỉ có CO2 phản ứng:
=> mdung dịch giảm = mCaCO3 – mCO2 => mCO2 = 2 – 0,68 = 1,32g
=> nCO2 = 1,32: 44 = 0,03 mol
- Xét phản ứng ban đầu:
C + H2O → CO + H2
Mol x → x → x
C +2H2O → CO2 + 2H2
Mol 0,03 → 0,06
Vậy hỗn hợp khí cuối cùng gồm: x mol CO và (x + 0,06) mol H2
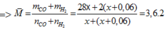
=> x = 0,02 mol
nKhí bđ = nCO2 + nCO + nH2 = 0,03 + 0,02 + 0,08 = 0,13 mol
=> Vkhí = 0,13.22,4 = 2,912 lit

Đáp án C
Phương pháp:
- Tính số mol CO và H2.
- m↓ - mCO2 = m dung dịch giảm => mCO2
- Viết PTHH. Tính toán theo PTHH.
Hướng dẫn giải:
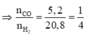
Ta có:



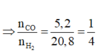
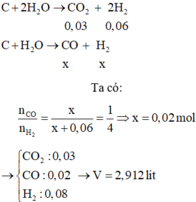

vì O2 không tác dụng với Ca(OH)2 nên chỉ có CO2 phản ứng
nCaCO3=\(\dfrac{1}{100}\)=0,01(mol)
PT: CO2+Ca(OH)2--> CaCO3+H2O
(mol)0,01<-0,01 <- 0,01 -> 0,01
tỉ lệ \(\dfrac{0,2}{1}\)>\(\dfrac{0,01}{1}\)=> Ca(OH)2 dư
nCa(OH)2 dư=0,2-0,01=0,19(mol)
PT:2CO2+Ca(OH)2-->Ca(HCO3)2
(mol)0,38 <- 0,19 -> 0,19
VCO2=(0,01+0,38).22,4=8,736(l)
%CO2=\(\dfrac{8,736}{10}\) .100%=87,36%
%O2=100%-87,36%=12,64%
p/s: mk không biết có đúng không nha
2,
nCa(OH)2=0,2.2=0,4(mol)
nCaCO3=\(\dfrac{30}{100}\)=0,3(mol)
PT: CO2+Ca(OH)2-->CaCO3+H2O
(mol)0,3 <- 0,3 <- 0,3 -> 0,3
VCO2(đktc)=0,3.22,4=6,72(l)