Nguyên tử Mg có ba đồng vị ứng 24Mg, 25Mg, 26Mg với thành phần phần trăm trong tự nhiên lần lượt là 78,6% ; 10,1% ; 11,3%
a) Tính nguyên tử khối trung bình của Mg
b) Giả sử trong một lượng Mg có 50 nguyên tử 25Mg, thì số nguyên tử tương ứng của hai đồng vị còn lại là bao nhiêu?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, Ta có : \(A=78,6\)%\(.24+10,1\)%.\(25+11,3\)%.\(26=24,327\)
b, \(24Mg\) 25Mg 26Mg
78,6% 10,1% 11,3%
\(x\) <--- 25 nguyên tử <-- \(y\)
Nhân chéo : \(x=\dfrac{25.78,6}{10} = 196,5 \) nguyên tử
\(y=\dfrac{25.11,3}{10} ≈28 \) nguyên tử

a) Đặt %24Mg là x
-->%25Mg là (100 - x - 11)
\(\overline{M}=\dfrac{x.24+\left(100-x-11\right).25+11.26}{100}=24,32\)
\(\Rightarrow x=\%^{24}Mg=79\%\)
b) ta có : \(n_{Mg}=n_{MgCl2}=1\left(mol\right)\Rightarrow n_{26_{Mg}}=1.11\%=0,11\left(mol\right)\)
Số nguyên tử : \(0,11.6,022.10^{-3}=6,6022.10^{-4}\)(nguyên tử)

Đáp án C
Nguyên tử khối trung bình của Mg là
MMg = ( 24 . 78 , 99 + 25 . 10 + 26 . 11 , 01 ) / 100 = 24 , 3202

Đáp án C.
Ta có:
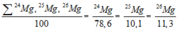
Giả sử trong hỗn hợp nói trên có 50 nguyên tử 25Mg, thì số nguyên tử tương ứng của 2 đồng vị còn lại là:
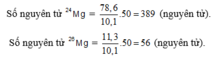

\(\overline{NTK}_{Mg}=\dfrac{24.98\%+25.2\%}{100\%}=24,02\left(đ.v.C\right)\\ \%m_{\dfrac{^{24}Mg}{MgCl_2}}=98\%.\dfrac{24,02}{24,02+35,5.2}\approx24,733\%\)

Ta có: \(\overline{A}=\dfrac{24\cdot69+25\cdot\left(100-69\right)}{100}=24,31\)
Gọi \(n_{MgCl_2}=1\left(mol\right)=n_{Mg}\) \(\Rightarrow n_{^{25}Mg}=0,31\left(mol\right)\)
\(\Rightarrow\%m_{^{25}Mg}=\dfrac{25\cdot0.31}{24,31+35,5\cdot2}\approx8,13\%\)

a)Nguyên tử khối trung bình của Mg là:
\(A_{Mg}=24\cdot\dfrac{78,6}{100}+25\cdot\dfrac{10,1}{100}+26\cdot\dfrac{11,3}{100}=24,33\)
b)Số nguyên tử \(^{24}MG=\dfrac{50}{10,1}\cdot78,6=389\) (nguyên tử)
Số nguyên tử \(^{26}Mg=\dfrac{50}{10,1}\cdot11,3=56\) (nguyên tử)
#khỏi ngủ trưa rồi (:|#